
可用于电动汽车的铝?空气燃料电池,通常以NaCl溶液或NaOH溶液为电解液,铝合金为负极,空气电极为正极。下列说法正确的是
A.以NaCl溶液或NaOH溶液为电解液时,正极反应式都为O2+2H2O+4e-==4OH-
B.以NaOH溶液为电解液时,负极反应式为Al+3OH-—3e-==Al(OH)3↓
C.以NaOH溶液为电解液时,电池在工作过程中电解液的pH保持不变
D.电池工作时,电子通过外电路从正极流向负极
科目:高中化学 来源: 题型:选择题
| A. | 1:2 | B. | 2:3 | C. | 3:1 | D. | 3:2 |
查看答案和解析>>
科目:高中化学 来源:2017届山东省高三上第一次教学诊断化学卷(解析版) 题型:填空题
I. 三氟化氮(NF3)是一种新型电子材料,它在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有:HF、NO和HNO3,请根据要求回答下列问题:
(1)反应过程中,被氧化与被还原的元素原子的物质的量之比为 。
(2)写出该反应的化学方程式_________________,若反应中生成0.2 mol HNO3,转移的电子数目为____________个。
(3)NF3是一种无色、无臭的气体,但一旦NF3在空气中泄漏,还是易于发现,你判断该气体泄漏时的现象是 。
(4)一旦NF3泄漏,可以用NaOH溶液喷淋的方法减少污染,其产物除NaNO2、NaF、H2O外,还肯定有__________(填化学式) 。
II.(1)已知Fe(OH)3能与次氯酸盐发生如下反应(未配平):Fe(OH)3+ClO-+OH-→FeO4n-+Cl-+H2O
①已知有10.7 g Fe(OH)3参加反应,共转移了0.3NA个电子,则n = ,FeO4n- 中铁元素的化合价为 。
② 根据所学的知识,推测FeO4n- 能和下列 (填序号)物质反应。
A.KMnO4 B.SO2 C.H2S D.O2
(2)一定条件下,含硝酸的废水中加入CH3OH,将HNO3还原成N2。若该反应消耗32 g CH3OH,转移6 mol电子,则参加反应的还原剂和氧化剂的物质的量之比是 。
查看答案和解析>>
科目:高中化学 来源:2017届山东省高三上第一次教学诊断化学卷(解析版) 题型:选择题
分类是化学学习与研究的常用方法,下列分类正确的是
A.Cl2O7、P2O5、SO3、CO2均属于酸性氧化物
B.Na2O、Na2O2为相同元素组成的金属氧化物,都属于碱性氧化物
C.根据是否具有丁达尔效应,将分散系分为溶液、浊液和胶体
D.根据溶液导电能力强弱,将电解质分为强电解质、弱电解质
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省高二上10月月考化学试卷(解析版) 题型:选择题
用如图所示的装置进行实验,反应一段时间后断开K,向右侧烧杯中加入0.1molCuO后CuSO4溶液恰好恢复到反应前的浓度和pH。下列说法中不正确的是
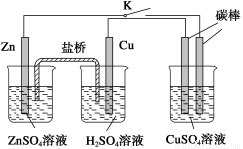
A.铜棒为正极,其电极反应式为2H++2e-==H2↑
B.烧杯右侧碳棒为阴极,其电极表面有红色物质析出
C.反应中消耗锌的质量为13g
D.导线中通过的电子的物质的量为0.2mol
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省高二上10月月考化学试卷(解析版) 题型:选择题
某课外活动小组,将剪下的一块镀锌铁片放入试剂瓶中,并滴入少量食盐水将其浸湿,再加数滴酚酞溶液,按如图装置进行实验,数分钟后观察,下列现象不可能出现的是
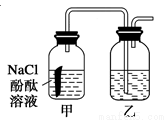
A.乙中导气管中产生气泡
B.乙中导气管里形成一段水柱
C.金属片剪口处溶液变红
D.锌被腐蚀
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省高二上第一次月考化学试卷(解析版) 题型:填空题
在一定条件下xA+yB zC达到平衡时,请填写:
zC达到平衡时,请填写:
(1)若A、B、C都是气体,在减压后平衡向逆反应方向移动,则x、y、z关系是______________。
(2)已知B、C是气体,现增加A的物质的量,平衡不移动,说明A是_____________(填状态)。
(3)若容器容积不变,加入气体B,气体A的转化率__________(填“增大”“减小”或“不变”)。
(4)若加热后,C的百分含量减小,则正反应是___________反应(填“放热”或“吸热”)。
(5)若容器容积不变,且A、B、C都是气体,向容器中充入稀有气体,则 。
A.化学平衡向正反应方向移动 B.化学平衡向逆反应方向移动
C.化学平衡不移动 D.反应停止
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省高二上第一次月考化学试卷(解析版) 题型:选择题
下列说法正确的是
A.强酸跟强碱的反应热一定是中和热
B.1molC完全燃烧放热383.3kJ,其热化学方程为:C+O2=CO2 ΔH=-383.3kJ·mol-1
C.在稀溶液中,酸与碱发生中和反应生成1 mol H2O时的反应热叫做中和热
D.表示中和热的离子方程式为:H+(aq)+OH-(aq) H2O(l)ΔH=57.3KJ·mol-1
H2O(l)ΔH=57.3KJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧气是氧化产物 | |
| B. | 还原剂与氧化剂的物质的量之比为1:4 | |
| C. | 若生成4.48 L HF,则转移0.8 mol电子 | |
| D. | O2F2既是氧化剂又是还原剂 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com