
���� ��1��SO2���ⵥ�ʻ�ԭΪI-����Ӧ���������HI��
��2��SO2�Ͱ�ˮ��Ӧ����SO32-���Ӷ�����BaSO3������SO2����ˮ�����ԣ��������Һ�е�NO3-�����������½�SO2����ΪSO42-���Ӷ�����BaSO4������SO2��������Һ��Ӧ���ɵ���ɫ�����ʣ�������
��3��X��S��O��������Ϊ2��3����S��O�����ʵ���֮����1��3��������XΪSO32-����ɱ�Cl2����ΪSO42-��
��4��ÿ����n��Cl-��=n��AgNO3��=a mol��n��BaCl2��=n��Na2SO4��=b mol������Cl-�غ㣬��n��KCl��=��a-2b��mol�����c=$\frac{n}{V}$����Ũ�ȣ�
��5��Qc��Ksp��AgCl���������г������ɣ�Ksp��AgCl����Ksp��AgI����AgCl��������ת��ΪAgI��
��� �⣺��1��SO2ͨ���ˮ�У���Һ��ɫ��ȥ������������ԭ��Ӧ���������HI����÷�Ӧ�����ӷ���ʽΪSO2+I2+2H2O�T4H++2I-+SO42-��
�ʴ�Ϊ��SO2+I2+2H2O�T4H++2I-+SO42-��
��2��A��SO2�Ͱ�ˮ��Ӧ����SO32-���Ӷ�����BaSO3��������Aѡ��
B�������������ᡢ�Ȼ���������Ӧ���������ɳ�������B��ѡ��
C��SO2����ˮ�����ԣ��������Һ�е�NO3-�����������½�SO2����ΪSO42-���Ӷ�����BaSO4��������Cѡ��
D��SO2��������Һ��Ӧ���ɵ���ɫ�����ʣ���������Dѡ��
�ʴ�Ϊ��ACD��
��3��X��S��O��������Ϊ2��3����S��O�����ʵ���֮����1��3����XΪSO32-��������ˮ���Լ��ԣ���ɱ�Cl2����ΪSO42-�����ӷ�ӦΪCl2+SO32-+H2O�TSO42-+2Cl-+2H+��
�ʴ�Ϊ���Cl2+SO32-+H2O�TSO42-+2Cl-+2H+��
��4��ÿ����n��Cl-��=n��AgNO3��=a mol��n��BaCl2��=n��Na2SO4��=b mol������Cl-�غ㣬��n��KCl��=��a-2b��mol��ÿ����Һ�������100 mL����ԭ���Һ��c��K+��=$\frac{��a-2b��mol}{0.1L}$=10��a-2b�� mol•L-1���ʴ�Ϊ��10��a-2b����
��5����0.1L 0.002mol•L-1��NaCl��Һ����μ���������0.1L 0.002mol•L-1��������Һ���а�ɫ�������ɣ�����c��Ag+��•c��Cl-��=10-6��Ksp��AgCl���������г������ɣ���Ӧ�����Һ�м�������0.1L0.002mol•L-1��NaI��Һ����Ksp��AgCl����Ksp��AgI����AgCl��������ת��ΪAgI����۲쵽��ɫ����ת��Ϊ��ɫ���������ӷ�ӦΪAgCl��s��+I-��aq���TAgI��s��+Cl-��aq����
�ʴ�Ϊ��c��Ag+��•c��Cl-����Ksp��AgCl������ɫ����ת��Ϊ��ɫ������AgCl��s��+I-��aq���TAgI��s��+Cl-��aq����
���� ���⿼����ۺϣ��漰������ԭ��Ӧ������ˮ�⼰���������ɺ�ת���ȣ����շ�Ӧԭ��Ϊ���Ĺؼ������ط�����Ӧ���������ۺϿ��飬��Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ʵ�鷽�� | ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
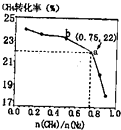 CH4����N2��һ����������ֱ�����ɰ���3CH4��g��+2N2��g��$?_{����}^{700��}$3C��s��+4NH3��g����H��0��700��ʱ��$\frac{n��C{H}_{4}��}{n��{N}_{2}��}$��CH4��ƽ��ת���ʵĹ�ϵ��ͼ��ʾ�������ж���ȷ���ǣ�������
CH4����N2��һ����������ֱ�����ɰ���3CH4��g��+2N2��g��$?_{����}^{700��}$3C��s��+4NH3��g����H��0��700��ʱ��$\frac{n��C{H}_{4}��}{n��{N}_{2}��}$��CH4��ƽ��ת���ʵĹ�ϵ��ͼ��ʾ�������ж���ȷ���ǣ�������| A�� | $\frac{n��C{H}_{4}��}{n��{N}_{2}��}$Խ��CH4��ת����Խ�� | |
| B�� | $\frac{n��C{H}_{4}��}{n��{N}_{2}��}$�벻��ʱ�����£�NH3������������С | |
| C�� | b���Ӧ��ƽ�ⳣ����a��Ĵ� | |
| D�� | a���Ӧ��NH3���������ԼΪ13% |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ʯ���ǻ���������Ʒ����Ҳ�ǻ���� | |
| B�� | NH4I�ĵ���ʽ��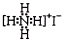 | |
| C�� | ���ࡢ�����ʺ����ᶼ����������Ӫ������ | |
| D�� | �մɡ�ˮ����ˮ�ࡢ���������ڹ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����O2��Ũ�����SO2��ת���� | |
| B�� | ���ø÷�Ӧ�ų���������SO2��O2Ԥ�� | |
| C�� | �����¶��ܼӿ췴Ӧ������ | |
| D�� | ��ʹ����ѹǿҲ����ʹSO2ȫ��ת��ΪSO3 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com