
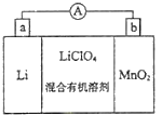
 如图是锂锰电池的反应原理示意图,其中电解质KClO4溶于混合有机溶剂中,Li+ 通过电解质迁移入MnO2晶格中,得到LiMnO2.回答下列问题:
如图是锂锰电池的反应原理示意图,其中电解质KClO4溶于混合有机溶剂中,Li+ 通过电解质迁移入MnO2晶格中,得到LiMnO2.回答下列问题:分析 (1)形成原电池反应时,Li为负极,被氧化,电极方程式为Li-e-=Li+,MnO2为正极,被还原,电极方程式为MnO2+e-+Li+=LiMnO2,结合电极方程式以及元素化合价的变化解答该题;
(2)①硝酸根离子为-1价,根据化合物中各元素化合价的代数和为0知,M元素在该化合物中化合价为+1价,电路中转移电子为0.4mol,则n(M)=n(e-)=0.4mol,M=$\frac{m}{n}$,数值上金属元素的摩尔质量等于其相对原子质量;
②根据“析出什么加入什么”原则加入物质,电解硫酸钾溶液时,阳极上析出氧气、阴极上析出氢气,所以相当于电解水,根据转移电子和析出物质之间的关系式计算;
③电解0.2molNaCl,氯离子完全放电转移电子物质的量为0.2mol,还有0.2mol电子是氢氧根离子转移的;电解过程分为两步:第一步电解反应式为2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+Cl2↑+H2↑、第二步电解反应式为2H2O$\frac{\underline{\;通电\;}}{\;}$O2↑+2H2↑,根据c(NaOH)计算溶液pH.
解答 解:(1)①Li为负极,MnO2为正极,原电池工作时,外电路的电流方向从正极到负极,即从b极流向a极,
故答案为:b;a;
②MnO2为正极,被还原,电极方程式为MnO2+e-+Li+=LiMnO2,故答案为:Li++MnO2+e-=LiMnO2;
(2)①硝酸根离子为-1价,根据化合物中各元素化合价的代数和为0知,M元素在该化合物中化合价为+1价,电路中转移电子为0.4mol,则n(M)=n(e-)=0.4mol,M=$\frac{m}{n}$=$\frac{43.2g}{0.4mol}$=108g/mol,数值上金属元素的摩尔质量等于其相对原子质量为108,故答案为:108;
②根据“析出什么加入什么”原则加入物质,电解硫酸钾溶液时,阳极上析出氧气、阴极上析出氢气,所以相当于电解水,生成1mol水转移电子2mol电子,则转移0.4mol电子生成n(H2O)=$\frac{0.4mol}{2}$×18g/mol=3.6g,需要进行的操作是向溶液中加入3.6g水即可,故答案为:向溶液中加入3.6g水;
③电解0.2molNaCl,氯离子完全放电转移电子物质的量为0.2mol,根据Cl原子守恒得n(Cl2)=$\frac{1}{2}$n(NaCl)=$\frac{1}{2}$×0.2mol=0.1mol,还有0.2mol电子是氢氧根离子转移的,生成n(O2)=$\frac{0.2mol}{4}$=0.05mol,则阳极生成气体体积=(0.1+0.05)mol×22.4L/mol=3.36L;电解过程分为两步:第一步电解反应式为2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+Cl2↑+H2↑、第二步电解反应式为2H2O$\frac{\underline{\;通电\;}}{\;}$O2↑+2H2↑,根据Na原子守恒得n(NaOH)=n(NaCl)=0.2mol,c(NaOH)=$\frac{0.2mol}{2L}$=0.1mol/L,则溶液pH=13,故答案为:3.36L;13.
点评 本题以电解原理为载体考查计算,为高频考点,明确各个电极上发生的反应是解本题关键,注意③题阳极产物成分及其物质的量,为易错点.


科目:高中化学 来源: 题型:解答题
 硫及其化合物广泛存在于自然界中,回答下列问题:
硫及其化合物广泛存在于自然界中,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 水泥、玻璃、水晶饰物都是硅酸盐制品 | |
| B. | 用澄清石灰水鉴别SO2 和CO2 | |
| C. | 将Fe(NO3)2 溶于稀盐酸,滴加KSCN 溶液没有颜色变化 | |
| D. | 透闪石的化学成分为Ca2Mg5Si8O22(OH)2 写成氧化物的形式为:2CaO•5MgO•8SiO2•H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 压强p/Pa | 2×105 | 5×105 | 1×106 |
| c(A)/mol•L-1 | 0.08 | 0.20 | 0.44 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在五水硫酸铜中滴加少量浓硫酸,固体颜色由蓝变白,说明浓硫酸具有吸水性 | |
| B. | 在未知试液中滴加BaCl2溶液得白色沉淀,取该白色沉淀加稀盐酸不溶解,说明原未知试液中含有SO42- | |
| C. | 在铜片上滴加少量稀硫酸,无明显现象,说明稀硫酸没有氧化性 | |
| D. | 某未知气体通入品红溶液中,品红溶液褪色,则原气体一定是 SO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2CO3溶液(NaHCO3),加入适量的NaOH溶液 | |
| B. | Na2CO3溶液(Na2SO4),加入适量的Ba(OH)2溶液后过滤 | |
| C. | NaHCO3溶液(Na2CO3),通入过量的CO2气体 | |
| D. | Na2O2粉末(Na2O),将混合物在空气中加热 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素代号 | A | B | D | E | G | H | I | J |
| 化合价 | -1 | -2 | +4、-4 | +4、-2 | +5、-3 | +3 | +2 | +1 |
| 原子半径/nm | 0.071 | 0.074 | 0.077 | 0.102 | 0.110 | 0.143 | 0.160 | 0.186 |
 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只含有1个双键的直链有机物 | B. | 含有2个双键的直链有机物 | ||
| C. | 含有1个双键的环状有机物 | D. | 含有1个叁键的直链有机物 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 需要加热才能发生的反应一定是吸热反应 | |
| B. | 放热反应在常温下一定很容易发生 | |
| C. | 反应是放热还是吸热,取决于反应物和生成物所具有的总能量的相对大小 | |
| D. | 在一定条件下,某可逆反应正向是吸热反应,则其逆向必是放热反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com