
| ||
| 1.5 |
| 11.2L-6.72L |
| 22.4L/mol |
| ||
| 1.5 |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、固体混合物中一定含有Al,但质量不可确定 | B、固体混合物中可能含有MgCl2和AlCl3 | C、固体混合物中一定含有MgCl2和FeCl2 | D、固体混合物中一定含有(NH4)2SO4、MgCl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
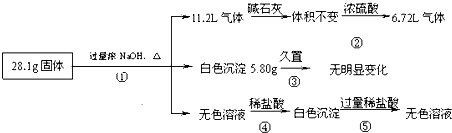
某固体混合物可能由SiO2、Fe2O3、A12O3、Na2SO3、Na2CO3中的两种或两种以上的物质组成。某兴趣小组为探究该固体混合物的组成,设计的部分实验方案如下图所示:
请回答下列问题:
(1)若试剂1是稀硫酸,试剂2是氢氧化钠溶液。在混合物样品中加以足量的稀硫酸后,固体全部溶解,得到混合气体A和澄清溶液B,在B中滴加过量氢氧化钠溶液时,先有沉淀生成,后沉淀部分溶解。则该混合物样品中一定不含的物质是 ;固体D的化学式为 ;检验混合物B中含有Fe3+所选用的试剂是 ;证明混合气体A中含有CO2的实验方法是 。
(2)若试剂1是水,试剂2是氢氧化钠溶液(过量)。在混合物样品中加足量的水后过滤,混合物B是滤渣,试推断:固体D的化学式为 ;检验溶液C中是否含有SiO32—的实验方法是 。
查看答案和解析>>
科目:高中化学 来源:2013-2014学年安徽省三校高三上学期12月联考理综化学试卷(解析版) 题型:选择题
某固体混合物可能由Al、(NH4)2SO4、MgCl2、FeCl2、AlCl3中的一种或几种组成,现对该混合物做如下实验,所得现象和有关数据如图所示(气体体积数据已换算成标准状况下的体积):
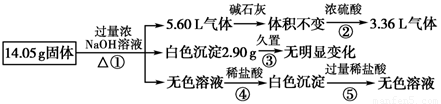
下列说法正确的是
A.固体混合物中一定含有Al,但质量不可确定
B.固体混合物中可能含有MgCl2和AlCl3
C.固体混合物中一定含有MgCl2和FeCl2
D.固体混合物中一定含有 (NH4)2SO4、MgCl2
查看答案和解析>>
科目:高中化学 来源:2015届黑龙江省高一上学期期末考试化学试卷(解析版) 题型:推断题
(4分)某固体混合物可能由K2SO4、NaCl、CuCl2和Na2SO3中的一种或几种组成.依次进行下列五步实验,观察到的现象记录如下:
①取一定量混合物加水溶解得无色透明溶液;
②向上述溶液中滴加足量BaCl2溶液,有白色沉淀生成,将该沉淀洗涤过滤干燥称得质量为a克;
③上述白色沉淀加入稀硝酸充分搅拌后,再次将沉淀洗涤过滤干燥称量,沉淀质量增加;
④往②的滤液中加入AgNO3溶液,有白色沉淀生成,该沉淀不溶于稀硝酸.根据以上实验现象,可以判断出混合物中肯定含有的物质是 ;肯定不含有的物质是 ;不能判断混合物中是否含有的物质是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com