
关于元素周期律和周期表的下列说法正确的是( )
A.目前发现的所有元素占据了周期表里全部位置,不可能再有新的元素被发现
B.元素的性质随着原子序数的增加而呈周期性变化
C.俄国化学家道尔顿为元素周期表的建立作出了巨大贡献
D.同一主族的元素从上到下,金属性呈周期性变化
 提分百分百检测卷系列答案
提分百分百检测卷系列答案 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案科目:高中化学 来源: 题型:
有机物G俗称PLA,在生产、生活用途前景广泛。它可由化合物A经过下列一系列反应制得,A中碳的质量分数为85.7%。
(已知含有醛基的有机物能与新制的氢氧化铜以及银氨溶液发生氧化还原反应)

(1)化合物F中所含官能团名称是_______________--。化合物H的结构简式___________________。
(2)在①—⑦的反应中,属于加成反应的有_________________。(填编号)
(3)写出符合下列条件的化合物E同分异构体__________________________。
①能与碳酸氢钠溶液反应,②能与银氨溶液反应
(4)写出反应③的化学方程式__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
利用反应2NO(g)+2CO(g)  2CO2(g)+N2(g) ΔH=-746.8 kJ/mol,可净化汽车尾气,如果要同时
2CO2(g)+N2(g) ΔH=-746.8 kJ/mol,可净化汽车尾气,如果要同时
提高该反应的速率和NO的转化率,采取的措施是( )
A.降低温度
B.增大压强同时加催化剂
C.升高温度同时充入N2
D.及时将CO2和N2从反应体系中移走
查看答案和解析>>
科目:高中化学 来源: 题型:
[选做题]本题有A、B两题,分别对应于“物质结构与性质”和“实验化学”两个选修课程模块的内容,每题12分。请选择其中一题作答,若两题都作答。将按A题评分。
A.【物质结构与性质】
可以由下列反应合成三聚氰胺:CaO+3C CaC2+CO↑,CaC2+N2
CaC2+CO↑,CaC2+N2  CN2+C,CaCN2+2H2O===NH2CN+Ca(OH)2,NH2CN与水反应生成尿素[CO(NH2)2],尿素合成三聚氰胺。
CN2+C,CaCN2+2H2O===NH2CN+Ca(OH)2,NH2CN与水反应生成尿素[CO(NH2)2],尿素合成三聚氰胺。
(1)写出与Ca在同一周期且最外层电子数相同、内层排满电子的基态原子的电子排布式: 。 CaCN2中阴离子为CN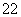 ,根据等电子原理可以推知CN
,根据等电子原理可以推知CN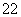 的空间构型为 。
的空间构型为 。
 (2)尿素分子中C原子采取 杂化。尿素分子的结构简式是 。
(2)尿素分子中C原子采取 杂化。尿素分子的结构简式是 。
(3)三聚氰胺( )俗称“蛋白精”。动物摄入三聚氰胺和三聚氰酸( )
后,三聚氰酸与三聚氰胺分子相互之间通过 结合,在肾脏内易形成结石。
(4)CaO晶胞如图所示,CaO晶体中Ca2+的配位数为 。
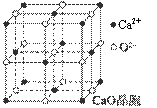

(5)CaO晶体和NaCl晶体的晶格能分别为:CaO 3401 kJ·mol-1、NaCl 786 kJ·mol-1。导致CaO比NaCl晶格能大的主要原因是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
在373 K时,密闭容器中充入一定量的NO2和SO2,发生如下反应:NO2+SO2 NO+SO3,下列叙述正确的是 ( )
NO+SO3,下列叙述正确的是 ( )
A.在任何时刻NO和SO3的物质的量一定相等
B.在平衡状态时NO2和SO2的物质的量一定相等
C.在任何时刻体系中的总物质的量一定等于反应开始时总物质的量
D.在平衡状态时SO2、NO2、NO、SO3的物质的量一定相等
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是 ( )
A.含有离子键的化合物必是离子化合物
B.含有共价键的化合物就是共价化合物
C.共价化合物可能含离子键
D.离子化合物中一定含有共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
下表是A、B、C、D、E五种有机物的有关信息:
| A | ①能使溴的四氯化碳溶液褪色;②比例模型为 |
| B | ①由C、H两种元素组成;②球棍模型为 |
| C | ①由C、H、O三种元素组成;②能与Na反应,但不能与NaOH溶液反应;③能与E反应生成相对分子质量为100的酯 |
| D | ①相对分子质量比C少2;②能由C氧化而成 |
| E | ①由C、H、O三种元素组成;②球棍模型为 |
回答下列问题:
(1)A与溴的四氯化碳溶液反应的生成物的名称是 。
(2)A与氢气发生加成反应后生成物质F,与F在分子组成和结构上相似的有机物有一大类(俗称“同系物”),它们均符合通式CnH2n+2。当n= 时,这类有机物开始出现同分异构体。
(3)B具有的性质是 (填序号)。
①无色无味液体 ②有毒 ③不溶于水 ④密度比水大 ⑤与酸性KMnO4溶液和溴水反应褪色 ⑥任何条件下都不与氢气反应
写出在浓硫酸作用下,B与浓硝酸反应的化学方程式:
。
(4)C与E反应能生成相对分子质量为100的酯,该反应的反应类型为 ;其化学方程式为 。
(5)写出由C氧化生成D的化学方程式:
。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com