
| A. | 0.1mol/L的氯化铁溶液中:Na+、K+、Br-、SCN- | |
| B. | 水电离出的氢氧根离子浓度为10-13mol/L的溶液中:NH4+、K+、SiO32-、SO42? | |
| C. | 使酚酞试液变红色的溶液中:Na+、K+、HCO3-、S2? | |
| D. | 澄清透明的溶液中:K+、Ca2+、MnO4-、NO3- |
分析 A.离子之间结合生成络离子;
B.水电离出的氢氧根离子浓度为10-13mol/L的溶液,为酸或碱溶液;
C.使酚酞试液变红色的溶液,显碱性;
D.该组离子之间不反应.
解答 解:A.Fe3+、SCN-结合生成络离子,不能大量共存,故A错误;
B.水电离出的氢氧根离子浓度为10-13mol/L的溶液,为酸或碱溶液,酸溶液中不能大量存在SiO32-,碱溶液中不能大量存在NH4+,故B错误;
C.使酚酞试液变红色的溶液,显碱性,不能大量存在HCO3-,故C错误;
D.该组离子之间不反应,可大量共存,故D正确;
故选D.
点评 本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重分析与应用能力的考查,注意复分解反应的判断,题目难度不大.


 考前必练系列答案
考前必练系列答案科目:高中化学 来源: 题型:多选题
| A. | 2,3-二氯丁烷 | B. | 1,3-二氯丁烷 | ||
| C. | 2-氯丁烷 | D. | 2,5-二氯己烷和1,2-二氯乙烷 |
查看答案和解析>>
科目:高中化学 来源:2017届江苏省如皋市高三上学期质量调研一化学试卷(解析版) 题型:选择题
下列有关化学用语表示正确的是
A.NH4Cl的电子式: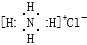
B.对硝基甲苯: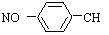
C.碳酸的电离方程式:H2CO3 2H++CO
2H++CO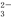
D.硫离子的结构示意图: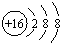
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向苯酚钠溶液中通入少量的SO2气体:C6H5O-+SO2+H2O→C6H5OH+HSO3- | |
| B. | 次氯酸钙溶液中通入过量二氧化碳:ClO-+H2O+CO2═HCO3-+HClO | |
| C. | 向NaHSO4溶液中滴加Ba(OH)2至溶液恰好呈现中性:Ba2++OH-+H++SO42-═BaSO4↓+H2O | |
| D. | 用惰性电极电解MgCl2溶液:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$2OH-+H2↑+Cl2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
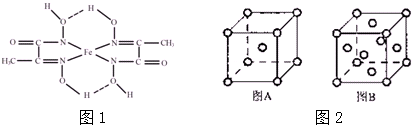
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
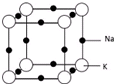 2015年8月12号接近午夜时分,天津滨海新区一处集装箱码头发生爆炸.发生爆炸的是集装箱内的易燃易爆物品,爆炸火光震天,并产生巨大蘑菇云.
2015年8月12号接近午夜时分,天津滨海新区一处集装箱码头发生爆炸.发生爆炸的是集装箱内的易燃易爆物品,爆炸火光震天,并产生巨大蘑菇云.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
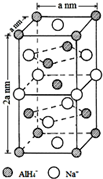 氢化铝钠(NaAlH4)是一种新型轻质储氢材料,掺入少量Ti的NaAlH4在150℃时释氢,在170℃、15.2MPa条件下又重复吸氢.NaAlH4可由AlCl3和NaH在适当条件下合成.NaAlH4的晶胞结构如图所示.
氢化铝钠(NaAlH4)是一种新型轻质储氢材料,掺入少量Ti的NaAlH4在150℃时释氢,在170℃、15.2MPa条件下又重复吸氢.NaAlH4可由AlCl3和NaH在适当条件下合成.NaAlH4的晶胞结构如图所示. .
.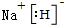 .
.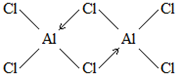 (标明配位键).
(标明配位键).查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com