
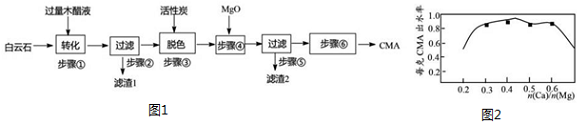
���� ��������ͼ��֪������ʯ����Ҫ�ɷ�MgCO3•CaCO3����SiO2�����ʣ���ľ��Һ����Ҫ�ɷ����ᣩ��Ӧ���ɴ���ƺʹ���þ�����˵�����1Ϊ�������裬��Һ����Ҫ�����Ǵ���ƺʹ���þ���������̼��ɫ���ټ�������þ��������Һ��n��Ca����n��Mg����ֵ�����ˣ���ȥ���Һ�й������ʣ��ô���ƺʹ���þ��Һ������Һ�����ᾧ�����ˡ�ϴ�Ӽ������CMA��
��1�������MgCO3•CaCO3��CH3COOH�ķ�Ӧ���ɴ���ƺʹ���þ��
��2����֪lmol NaOH��������跢����Ӧʱ�ų�����ΪQkJ����Ӧ���Ȼ�ѧ����ʽΪSi02��s��+2NaOH��aq��=Na2SiO3��aq��+H2O��l������H=-2QkJ/mol��
�����������Һ���ʺ�ɫ����ɫ����ľ��Һ�к�����������ɫ�Ľ����й��⣬������ɫ����һ��Ҫԭ����ʵ������б��ӱ������������������ղ�����ɫ���ʣ�
��3��������ͼ2��ʾ�ơ�þ�����ʵ���֮�����ˮ�ʣ�����ѩЧ�������ȣ���ϵ����֪����n��Ca����n��Mg��ԼΪ3��7ʱ����ˮ����ߣ�
��4����������ķ�����֪������ް����IJ����� �����ᾧ�����ˡ�ϴ�Ӽ����
��5��ȡakg��MgC03•CaC03��������Ϊb%�İ���ʯ���������������Ʊ�CMA����֪MgC03'•CaC03����ʧ��Ϊc%����ɵ�n��Ca��CH3COO��2��=$\frac{a��b%��1-c%��}{184}$��103mol��
n��Mg��CH3COO��2��=$\frac{a��b%��1-c%��}{184}$��103��$\frac{7}{3}$mol�������֮��ƷCMA����ʧ��Ϊd%���Դ˼��������
��� �⣺��1������ٷ����ķ�Ӧ���ӷ���ʽΪ MgCO3•CaCO3+4CH3COOH=Ca2++Mg2++4CH3COO-+2CO2��+2H2O��
�ʴ�Ϊ��MgCO3•CaCO3+4CH3COOH=Ca2++Mg2++4CH3COO-+2CO2��+2H2O��
��2����֪lmol NaOH��������跢����Ӧʱ�ų�����ΪQkJ����Ӧ���Ȼ�ѧ����ʽΪSi02��s��+2NaOH��aq��=Na2SiO3��aq��+H2O��l������H=-2QkJ/mol��
�����������Һ���ʺ�ɫ����ɫ����ľ��Һ�к�����������ɫ�Ľ����й��⣬������ɫ����һ��Ҫԭ����ʵ������б��ӱ������������������ղ�����ɫ���ʣ�
�ʴ�Ϊ��Si02��s��+2NaOH��aq��=Na2SiO3��aq��+H2O��l������H=-2QkJ/mol��ʵ������б��ӱ������������������ղ�����ɫ���ʣ�
��3��������ͼ2��ʾ�ơ�þ�����ʵ���֮�����ˮ�ʣ�����ѩЧ�������ȣ���ϵ����֪����n��Ca����n��Mg��ԼΪ3��7ʱ����ˮ����ߣ����Բ���ܵ�Ŀ�ij�����n��Ca����n��Mg��ԼΪ3��7��������м�������þ��Ŀ���ǵ��ڸơ�þ���ӵ����ʵ���֮�ȣ���ȥ���������ᣬ
�ʴ�Ϊ��C����ȥ���������
��4����������ķ�����֪������ް����IJ����� �����ᾧ�����ˡ�ϴ�Ӽ����
�ʴ�Ϊ�������ᾧ��
��5��ȡakg��MgC03•CaC03��������Ϊb%�İ���ʯ���������������Ʊ�CMA����֪MgC03'•CaC03����ʧ��Ϊc%����ɵ�n��Ca��CH3COO��2��=$\frac{a��b%��1-c%��}{184}$��103mol��
n��Mg��CH3COO��2��=$\frac{a��b%��1-c%��}{184}$��103��$\frac{7}{3}$mol�������֮��ƷCMA����ʧ��Ϊd%�����֪���ò�Ʒ����ԼΪ��$[\frac{a��b%����1-c%����158}{184}+\frac{a��b%����1-c%����\frac{7}{3}��142}{184}]����1-d%��$��
�ʴ�Ϊ��$[\frac{a��b%����1-c%����158}{184}+\frac{a��b%����1-c%����\frac{7}{3}��142}{184}]����1-d%��$��
���� ���⿼��CMA�Ĺ������̣����ؿ���ѧ���Ķ���Ŀ��ȡ��Ϣ�������Թ������̵����⡢���ʷ����ᴿ���������Ƶȣ��ۺ��Խ�ǿ����Ŀ�Ѷ��еȣ���Ҫѧ���߱���ʵ�Ļ���֪ʶ���ۺ�����֪ʶ����Ϣ���н�������������


 ����ѧ��Ӧ�����ϵ�д�
����ѧ��Ӧ�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
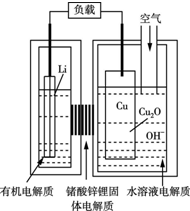 ��������ѧ����������һ�ָ��������ͳɱ��-ͭ����ȼ�ϵ�أ��õ��ͨ��һ�ָ��ӵ�ͭ��ʴ����������������зŵ����Ϊ2Li+Cu2O+H2O=2Cu+2Li++2OH��������˵������ȷ���ǣ�������
��������ѧ����������һ�ָ��������ͳɱ��-ͭ����ȼ�ϵ�أ��õ��ͨ��һ�ָ��ӵ�ͭ��ʴ����������������зŵ����Ϊ2Li+Cu2O+H2O=2Cu+2Li++2OH��������˵������ȷ���ǣ�������| A�� | �ŵ�ʱ������ͨ������������Cu���ƶ� | |
| B�� | ͨ����ʱ��ͭ����ʴ���������Cu2O | |
| C�� | �ŵ�ʱ�������ĵ缫��ӦʽΪCu2O+H2O+2e��=2Cu+2OH�� | |
| D�� | ������Ӧ�����У�ͭ�൱�ڴ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��Ũ�ȵĢ٣�NH4��2SO4��Һ����NH4HCO3��Һ����NH4Cl��Һ�е�c��NH4+�����٣��ۣ��� | |
| B�� | �����pH=a�Ĵ�����pH=b��NaOH��Һ��a+b=14����ֻ��ʱ�������У�c��CH3COO-����c��Na+����c��H+����c��OH-�� | |
| C�� | ��֪Ka��HClO��=3.0��10-8��Ka��HCN��=6.2��10-10�����������Ũ�ȵ�NaClO��NaCN��Һ�У�ǰ���е���������С�ں����е��������� | |
| D�� | ��20mL��ˮ�м���10mL��Ũ�ȵ����ᣬ��c��NH4+��-c��NH3•H2O��=2[c��OH-��-c��H+��] |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 | 0 | 20 | 40 | 60 | 80 | 100 | 120 |
| T1 | 2100 | 1052 | 540 | 199 | 8.7 | 0.06 | 0.06 |
| T2 | 2100 | 869 | 242 | x | x | x | x |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
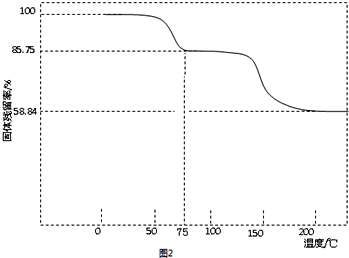
| ʵ������ | ʵ�鷽�� | ʵ������ԭ����� |
| �ٵ�����Ũ�������ƽ���Ӱ�� | ȡPbI2������Һ������һ֧�Թ��У��ٵ��뼸��NaI������Һ | ������Һ��c��I-������ʹQ������PbI2��Ksp |
| ��Ǧ����Ũ�ȼ�С��ƽ���Ӱ�� | ȡPbI2����Һ������һ֧�Թ��У��ټ�������NaCl������Һ | ����ɫ������ʧ ԭ���γ�PbCl42-��������Һ��c��Pb2+����С��ʹQcС��PbI2��Ksp |
| ��Ǧ���Ӻ͵�����Ũ�ȶ���С��ƽ���Ӱ�� | ��PbI2����Һ�е��뼸��FeCl3������Һ | ����ɫ������ʧ д����Ӧ�����ӷ���ʽ��PbI2+2Fe3++4Cl-=PbCl42-+2Fe2++I2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢ڢܢ� | B�� | �ۢ� | C�� | �ۢܢ� | D�� | �ڢۢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
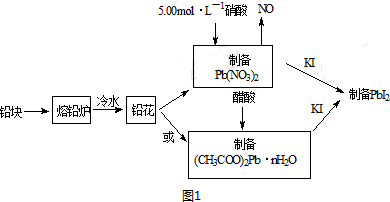
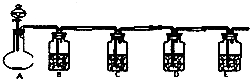 ���һʵ�齫ֻ����Na2SO4��Na2SO3��Na2CO3�İ�ɫ�����е����ֳɷּ��������ȡһ�����İ�ɫ��������ƿA�У�ͨ����Һ©������Һ��a����ͼ��ʾ��
���һʵ�齫ֻ����Na2SO4��Na2SO3��Na2CO3�İ�ɫ�����е����ֳɷּ��������ȡһ�����İ�ɫ��������ƿA�У�ͨ����Һ©������Һ��a����ͼ��ʾ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | 25��ʱ��pH=7��NH4Cl��NH3•H2O�����Һ�У�c��H+��=c��OH-����c��NH4+��=c��Cl-�� | |
| B�� | ��pH=3�Ĵ�����Һϡ�ͺ���Һ���������ӵ�Ũ�Ⱦ����� | |
| C�� | ��Na2CO3��Һ����εμ�ϡ����ʱ����Һ��c��HCO3-���ı仯������ȱ�С���� | |
| D�� | 0.01 mol•L-1Na2CO3��Һ��0.01 mol•L-1 NaHCO3��Һ�������ϣ�3c��CO32-��+3c��HCO3-��+3c��H2CO3��=2c��Na+�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
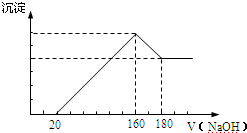
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com