
| A. | 需要加热才能发生的反应,一定是吸热反应 | |
| B. | 1mol酸与碱恰好中和时所放出的热量叫中和热 | |
| C. | 化学反应中的能量变化都表现为热量的变化 | |
| D. | 化学反应中的能量变化,主要是由化学键的变化引起的 |
分析 A.反应条件与反应热没有必然关系,需要加热才能进行的化学反应不一定是吸热反应;
B.中和热是强酸强碱的稀溶液完全反应生成1mol水放出的热量;
C.化学反应能量变化有热能、光能、电能、机械能等多种;
D.化学反应的实质是旧化学键断裂,新化学键的形成过程.
解答 解:A.需要加热才能进行的化学反应不一定是吸热反应,如铝热反应,需要加热,但属于放热反应,故A错误;
B.中和热是强酸强碱的稀溶液完全反应生成1mol水放出的热量,酸碱分强弱,一元、二元之分,1mol酸与碱恰好中和时不一定生成1mol水,故B错误;
C.化学反应中的能量多数主要以热的形式释放,但还可表现为热能、光能、电能、机械能等多种,故C错误;
D.化学反应的实质是旧化学键断裂,新化学键的形成过程,一定伴随能量变化,则化学反应中的能量变化主要是由化学键变化引起的,故D正确;
故选D.
点评 本题考查反应热与能量变化,题目难度不大,注意能量的表现形式以及常见吸热反应、放热反应,试题侧重基础知识的考查,有利于提高学生的分析能力及灵活应用能力.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
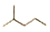 ,其分子式为C6H14,名称是2-甲基戊烷,它可由2种炔通过加成反应得到.
,其分子式为C6H14,名称是2-甲基戊烷,它可由2种炔通过加成反应得到.| 实验步骤 | 解 释 或 实 验 结 论 |
| (1)称取A 18.0g,升温使其汽化,测其密度是相同条件下H2的45倍. | ①A的相对分子质量为90. |
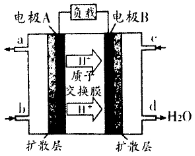
(2)A的核磁共振氢谱如图: | ②A中含有4种氢原子. |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含有2个羧基 | B. | 含有1个甲基 | ||
| C. | 含有2个羟基 | D. | 同时含有1个羟基和1个醛基 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
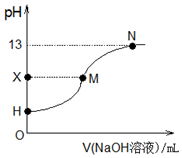
| A. | 酸碱滴定选用指示剂:甲基橙试液 | |
| B. | H点处的溶液:pH<3 | |
| C. | X=7时,M点对应加入氢氧化钠溶液的体积:25.00 mL | |
| D. | H、M、N三点各自对应的溶液:c(Na+)+c(H+)=c(CH3COO-)+c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;R2Q2与X2Q反应的化学方程式为2Na2O2+2H2O=4NaOH+O2↑.
;R2Q2与X2Q反应的化学方程式为2Na2O2+2H2O=4NaOH+O2↑.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硝酸与铜反应得到NO2、N2O4共23g,则铜失去的电子数为0.5NA | |
| B. | 10g 46%的乙醇水溶液中所含氢原子数目为0.6NA | |
| C. | 标准状况下8.96L的平均相对分子质量为3.5的H2与D2含有中子数0.3NA | |
| D. | 1molCu与足量的S完全反应,转移电子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
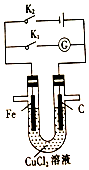
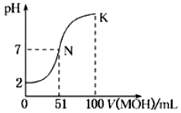
| A. | 同时打开K1、K2,铁棒上有紫红色物质析出 | |
| B. | 只闭合K1,石墨棒上有紫红色物质析出 | |
| C. | 只闭合K2,当电路中通过0.3mol电子时,两极共产生4.48L(标准状况)气体 | |
| D. | 只闭合K2,一段时间后,将电解质溶液搅拌均匀,溶液的pH变大(不考虑Cl2的溶解) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com