
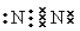 ��
��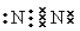 ���ʴ�Ϊ��7
���ʴ�Ϊ��7 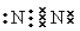 ��
��

 ÿ��10���ӿ�����������������ϵ�д�
ÿ��10���ӿ�����������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 �����ǵ�ѭ���е���Ҫ���ʣ�����������������������Ź㷺��Ӧ�ã�������ѧ֪ʶ���ݴ��������Ҫ��
�����ǵ�ѭ���е���Ҫ���ʣ�����������������������Ź㷺��Ӧ�ã�������ѧ֪ʶ���ݴ��������Ҫ��| ��ѧʽ | CO��g�� | H2��g�� | CH3OH��l�� | CH4��g�� |
| ��H/��kJ/mol�� | -283.0 | -285.8 | -726.5 | -890.3 |
| 3 |
| 2 |
| 3 |
| 2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| ||
| ���� |
| ||
| ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ʵ���� | T���棩 | n ��N2��/n��H2�� | P��MPa�� | ƽ��ʱNH3�ٷֺ��� |
| �� | 450 | 1/3 | 1 | |
| �� | �� | 1/3 | �� | |
| �� | 480 | 1/3 | 10 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
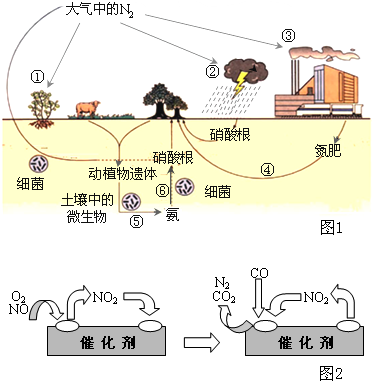 ���������Ļ��������ڴ����ŵ���ѭ�������������������������������������������������������ͼ1����Ȼ���е���ѭ��ͼ����ش��й����⣮
���������Ļ��������ڴ����ŵ���ѭ�������������������������������������������������������ͼ1����Ȼ���е���ѭ��ͼ����ش��й����⣮
| ||
| ||
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com