
【题目】铅是一种金属元素,可用作耐酸腐蚀、蓄电池等的材料。其合金可作铅字、轴承、电缆包皮之用,还可做体育运动器材铅球等。
(1)铅元素位于元素周期表第六周期IVA。IVA中原子序数最小的元素的原子有_______种能量不同的电子,其次外层的电子云有_______种不同的伸展方向。
(2)与铅同主族的短周期元素中,其最高价氧化物对应水化物酸性最强的是______(填化学式),气态氢化物沸点最低的是_____________(填化学式)。
(3)配平下列化学反应方程式,把系数以及相关物质(写化学式)填写在空格上, 并标出电子转移的方向和数目。
__PbO2+___MnSO4+___HNO3 →___HMnO4+___Pb(NO3)2+___PbSO4↓+____ ____
(4)把反应后的溶液稀释到1 L,测出其中的Pb2+的浓度为0.6 mol·L-1,则反应中转移的电子数为_______个。
(5)根据上述反应,判断二氧化铅与浓盐酸反应的化学方程式正确的是_______
A. PbO2+4HCl→PbCl4+2H2O B. PbO2+4HCl→PbCl2+ Cl2↑+2H2O
C. PbO2+2HCl+2H+→PbCl2+2H2O D. PbO2+4HCl→PbCl2+2OH-
【答案】3 1 H2CO3 CH4 5 2 6 2 3 2 2H2O 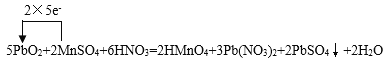 2NA B
2NA B
【解析】
(1)IVA中原子序数最小的元素的原子为C,其核外电子排布式为1s22s22p2,则碳原子有1s、2s和3p三种能量不同的电子;C的次外层为s轨道,为球形对称结构;
(2)元素的非金属性越强,其最高价氧化物对应的水化物酸性越强;同一主族元素中,氢化物的相对分子质量越大,分子间作用力越大,其沸点越高;
(3)根据氧化还原反应中化合价升降相等配平,然后利用单线桥表示出该反应中电子转移的方向和数目;
(4)根据n=c·V计算出铅离子的物质的量,根据反应计算出硫酸铅的物质的量,再根据化合价变化计算出转移电子的物质的量及数目;
(5)根据(3)可知二氧化铅的氧化性大于氯气,二氧化铅与浓盐酸发生氧化还原反应生成氯化铅、氯气和水,据此进行判断。
(1)IVA中原子序数最小的元素为C,C原子核外有6个电子,其核外电子排布式为1s22s22p2,则碳原子有1s、2s和3p三种能量不同的电子;C的次外层为1s轨道,为球形对称结构,只存在1种不同的伸展方向;
(2)IVA中非金属性最强的为C,则其最高价氧化物对应的水化物的酸性最强,该物质为碳酸,其化学式为:H2CO3;
对于结构相似的物质,相对分子质量越大,分子间作用力越大,物质的熔沸点就越高。IVA族元素中,CH4的相对分子质量最小,则其沸点最低;
(3)PbO2中Pb的化合价从+4变为+2价,化合价降低2价;MnSO4中锰元素化合价从+2变为+7,化合价升高5价,则化合价变化的最小公倍数为10,所以二氧化铅的系数为5,硫酸锰的稀释为2,然后利用质量守恒定律可知生成物中未知物为H2O,配平后的反应为:5PbO2+2MnSO4+6HNO3=2HMnO4+3Pb(NO3)2+2PbSO4↓+2H2O,用单线桥表示电子转移的方向和数目为: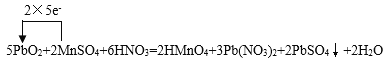 ;
;
(4)把反应后的溶液稀释到1 L,测出其中的Pb2+的浓度为0.6 mol/L,则反应生成铅离子的物质的量为:n(Pb2+)=c·V=0.6 mol/L×1 L=0.6 mol,硫酸铅中铅离子的物质的量为0.4 mol,则反应中转移电子的物质的量为:(0.6+0.4) mol×(4-2)=2 mol,反应转移电子的数目为2NA;
(5)根据(3)可知氧化性:PbO2>HMnO4,而HMnO4能够氧化Cl-,所以PbO2能够氧化Cl-,二者反应的化学方程式为:PbO2+4HCl→PbCl2+Cl2↑+2H2O,故合理选项是B正确。


科目:高中化学 来源: 题型:
【题目】对于可逆反应 N2(g)+3H2(g)2NH3(g) △H<0,下列研究目的和图示相符的是
A.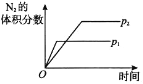 压强对反应的影响(p2>p1)
压强对反应的影响(p2>p1)
B.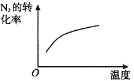 温度对反应的影响
温度对反应的影响
C.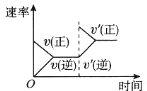 平衡体系增加 N2对反应的影响
平衡体系增加 N2对反应的影响
D.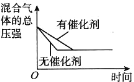 催化剂对反应的影响
催化剂对反应的影响
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以天然气、焦炭、水为初始原料,可以制得CO和H2,进而人工合成汽油。(流程示意图如下,反应③的H2也由反应①得到。)
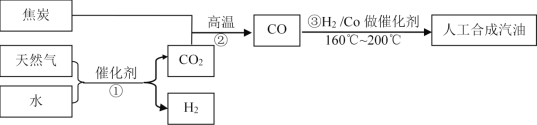
若反应①、②、③的转化率均为100%,且将反应①中得到的CO2和H2全部用于合成人工汽油。
(1)通过计算说明上述方案能否得到理想的产品_______________。
(2)当CO2的使用量应控制为反应①中CO2产量的______________(填比例范围),可以得到理想的产品。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于各图的说法(其中①③④中均为情性电极)正确的是( )
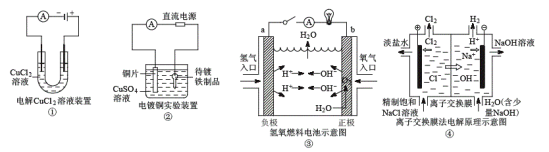
A.①装置中阴极处产生的气体能够使湿润KI淀粉试纸变蓝
B.②装置中待镀铁制品应与电源正极相连
C.③装置中电子由b极流向a极
D.④装置中的离子交换膜可以避免生成的Cl2与NaOH溶液反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用下图装置测定中和热的实验步骤如下:

①量取50mL 0.25mol/L H2SO4溶液倒入小烧杯中,测量温度;
②量取50mL 0.55mol/L NaOH溶液,测量温度;
③将NaOH溶液倒入小烧杯中,混合均匀后测量混合液温度。请回答:
(1)如图所示,仪器A的名称是_______________;
(2)NaOH溶液稍过量的原因 ______________。
(3)加入NaOH溶液的正确操作是_______(填字母)。
A.沿玻璃棒缓慢加入 B.一次迅速加入 C.分三次加入
(4)使硫酸与NaOH溶液混合均匀的正确操作是 _________________________。
(5)实验数值结果与57.3 kJ/mol有偏差,产生偏差的原因可能是(填字母)______
a.实验装置保温、隔热效果差
b.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
c.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ClO2是一种高效、广谱、安全的杀菌、消毒剂,易溶于水。制备方法如下:
(1)步骤Ⅰ:电解食盐水制备氯酸钠。用于电解的食盐水需先除去其中的 Ca2+、Mg2+、SO42-等杂质。在除杂操作时,往粗盐水中先加入过量的________(填化学式),至沉淀不再产生后,再加入过量的________和NaOH,充分反应后将沉淀一并滤去。
(2)步骤Ⅱ:将步骤Ⅰ得到的食盐水在特定条件下电解得到氯酸钠(NaClO3),再将它与盐酸反应生成ClO2与Cl2,ClO2与Cl2的物质的量比是____________。
(3)学生拟用左下图所示装置模拟工业制取并收集ClO2,用NaClO3和草酸(H2C2O4)恒温在60℃ 时反应制得。

反应过程中需要对A容器进行加热,加热的方式为____________;加热需要的玻璃仪器除酒精灯外,还有_________________;
(4)反应后在装置C中可得亚氯酸钠(NaClO2)溶液。已知NaClO2饱和溶液在温度低于38℃时,析出的晶体是NaClO2·3H2O,在温度高于38℃时析出的是NaClO2。根据右上图所示NaClO2的溶解度曲线,请完成从NaClO2溶液中制得NaClO2·3H2O的操作步骤:
①_____________;②_______________;③洗涤;④干燥。
(5)目前我国已成功研制出利用NaClO2制取二氧化氯的新方法,将Cl2通入到NaClO2溶液中。现制取270kg二氧化氯,需要亚氯酸钠的质量是________。
(6)ClO2和Cl2均能将电镀废水中的剧毒CN-氧化为无毒物质,自身被还原为Cl-。处理含CN-相同量的电镀废水,所需Cl2的物质的量是ClO2的_______倍。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】3-羟基丁酸(3-hydroxybutyrate)也称为β-羟基丁酸(beta-hydroxybutyrate),在工业中可用于合成可生物降解的塑料,如聚(3-羟基丁酸)。
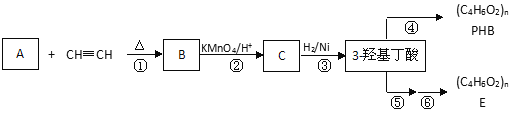
已知:i. 共轭二烯烃(如异戊二烯)与含有碳碳叁键的有机物作用时能形成环状化合物:
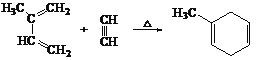
ii. 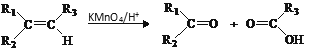
iii. 步骤②只有一种产物;E的结构中含有甲基
(1)A分子结构简式 _______;理论上B也可以由1,3-丁二烯与烃F来合成,则F的名称(系统命名法):_________;C中含有的官能团是_______(用符号表示)。
(2)写出反应类型:②_____________, ④_____________。
(3)PHB______(填“有”或“无”)固定熔沸点;它与E______(填“互为”或“不互为”)同分异构体。下列有机物具有类似共轭二烯烃性质的是__________(填序号);
a. ![]() b.
b. ![]()
c. ![]() d.
d. 
(4)写出反应⑤的化学方程式________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】普通电解精炼铜的方法所制备的铜中仍含杂质,利用下面的双膜( 阴离子交换膜和过滤膜)电解装置可制备高纯度的Cu。下列有关叙述正确的是

A. 电极a为粗铜,电极b为精铜
B. 甲膜为过滤膜,可阻止阳极泥及漂浮物杂质进入阴极区
C. 乙膜为阴离子交换膜,可阻止杂质阳离子进入阴极区
D. 当电路中通过1mol电子时,可生成32g精铜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】浓度均为0.1mol/L的下列各组溶液,将溶液(Ⅱ)滴加到溶液(Ⅰ)中,测得溶液(I)的导电能力变化符合如图变化趋势的是( )
A | B | C | D | |
溶液(Ⅰ) | 盐酸 | 醋酸 | 氢氧化钠 | 氨水 |
溶液(Ⅱ) | 氢氧化钠 | 氢氧化钠 | 氨水 | 硝酸银 |
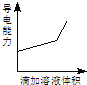
A.AB.BC.CD.D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com