
【题目】海带、紫菜中均含有丰富的碘元素,从海带中提取碘单质的流程如下,思考解答下列问题:

(1)实验操作③的名称是______。
(2)根据元素周期表中元素性质的递变规律,实验操作④反应的离子方程式是______。
(3)实验操作⑤中不选用酒精的理由:_______。
(4)为使海带灰中碘离子转化为碘的有机溶液,实验室里有烧杯玻璃棒、集气瓶、酒精灯、导管、圆底烧瓶、石棉网以及必要的夹持仪器物品,尚缺少的玻璃仪器是_____。
【答案】过滤 2I-+Cl2==I2+2Cl-或2I- +Br2==I2+2Br- 酒精与水互溶 漏斗、分液漏斗
【解析】
海带晒干灼烧可生成水和二氧化碳,海带灰中含有碘化钾等物质,溶于水,浸泡过滤得到含有碘离子的溶液,加入氯水或通入氯气,氯气置换出碘,得到碘的水溶液,用四氯化碳萃取得到含碘的有机溶液,最后蒸馏可得到碘,以此解答该题。
(1) 将悬浊液分离为残渣和含碘离子溶液应选择过滤的方法;
(2)卤素单质X2的氧化性随核电荷数的递增而减弱,氧化溶液中的I-生成I2,可选择氯气或Br2,则操作④发生反应的离子方程式是2I-+Cl2==I2+2Cl-或2I- +Br2==I2+2Br-;
(3)萃取碘水中的I2,萃取剂不能溶于水,而酒精与水互溶,则操作⑤中不能选用酒精作萃取剂;
(4)为使海藻灰中碘离子转化为碘的有机溶液,根据实验装置原理,基本操作有过滤、萃取分液、使用的仪器有:烧杯、玻璃棒、漏斗,分液漏斗等,尚缺少的玻璃仪器是(普通)漏斗和分液漏斗。


科目:高中化学 来源: 题型:
【题目】可逆反应aA(g)+bB(s)![]() cC(g)+dD(g),其他条件不变,C的物质的量分数和温度(T)或压强(P)关系如图,其中正确的是( )
cC(g)+dD(g),其他条件不变,C的物质的量分数和温度(T)或压强(P)关系如图,其中正确的是( )

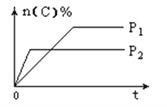
A. 升高温度,平衡向正反应方向移动 B. 使用催化剂,C的物质的量分数增加
C. 化学方程式系数a<c+d D. 根据图象无法确定改变温度后平衡移动方向
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用0.10mol·L-1NaOH溶液分别滴定20.00mL浓度均为0.10 mol·L-1CH3COOH
溶液和HCN溶液所得滴定曲线如右图。下列说法正确的是

A. 点①和点②所示溶液中:c(CH3COO-)<c(CN-)
B. 点③和点④所示溶液中:c(Na+)>c(OH-)>c(CH3COO-)>c(H+)
C. 点①和点②所示溶液中:c(CH3COO-)-c(CN-)=c(HCN)-c(CH3COOH)
D. 点②和点③所示溶液中都有:c(CH3COO-)+c(OH-)=c(CH3COOH)+c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有物质的量浓度均为![]() 的①
的①![]() 溶液 ②
溶液 ②![]() 溶液③
溶液③ ![]() 溶液各25mL,下列说法正确的是
溶液各25mL,下列说法正确的是
A.3种溶液pH的大小顺序是③>②>①
B.若将3种溶液稀释相同倍数,pH变化最大的是①
C.若分别加入25mL ![]() 盐酸后,pH最小的是②
盐酸后,pH最小的是②
D.若升高温度,则③的pH不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A. 0.1 mol/LC6H5ONa溶液中:c(Na+)>c(C6H5O-)>c(H+)>c(OH-)
B. Na2CO3溶液加水稀释后,恢复至原温度,pH和Kw均减小
C. pH=5的CH3COOH溶液和pH=5的NH4Cl溶液中,c(H+)不相等
D. 在Na2S溶液中加入AgCl固体,溶液中c(S2-)下降
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是锂电池放电的装置图,电池反应为4Li+FeS2=Fe+2Li2S,LiPF6是电解质,SO(CH3)2是溶剂。下列说法正确的是( )

A.a极是正极B.电子从b极流出经外电路流入a极
C.Li+向b极迁移D.可用水代替SO(CH3)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B两个完全相同的装置,某学生分别在它们的侧管中装入![]()
![]() 和
和![]()
![]() ,A、B中分别有10mL相同浓度的盐酸(不考虑盐酸的挥发),将两个侧管中的物质同时倒入各自的试管中,下列叙述正确的是( )
,A、B中分别有10mL相同浓度的盐酸(不考虑盐酸的挥发),将两个侧管中的物质同时倒入各自的试管中,下列叙述正确的是( )

A.B装置的气球膨胀的体积大
B.最终两试管中NaCl的物质的量一定相同
C.若最终两气球体积不同,则盐酸的浓度一定小于或等于![]()
D.若最终两气球体积相同,则盐酸的浓度一定大于或等于![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化氢一定条件下可发生分解:2H2O2(l)=2H2O(l)+O2(g),其能量变化如下图所示,下列说法正确的是
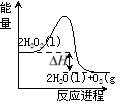
A.该分解反应为吸热反应
B.2molH2O2具有的能量小于2molH2O和1molO2所具有的总能量
C.加入MnO2或FeCl3均可提高该分解反应的速率
D.其他条件相同时,H2O2溶液的浓度越大,其分解速率越慢
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应3Fe(s)+4H2O(g)![]() Fe3O4(s)+4H2(g)的平衡常数,下列说法正确的是
Fe3O4(s)+4H2(g)的平衡常数,下列说法正确的是
A. K=![]()
B. K=![]()
C. 增大c(H2O)或减小c(H2),会使该反应平衡常数减小
D. 改变反应的温度,平衡常数不一定变化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com