
标准状况下,ag气体A和bg气体B的分子数相同,下列说法不正确的是
A.气体A和B的相对分子质量之比为 a:b
B.同质量的气体A和B所含分子数目之比为b:a
C.标准状况下,气体A和B的密度之比为b:a
D.相同条件下,等体积的气体A和B的质量之比为a:b
 轻松暑假总复习系列答案
轻松暑假总复习系列答案科目:高中化学 来源:2014-2015学年广东省汕头市高二上学期期中化学(文)试卷(解析版) 题型:?????
下列食物中富含维生素C的是
A.食用油 B.蔗糖 C.西红柿 D.鸡蛋
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省汕头市高二上学期期中化学(理)试卷(解析版) 题型:选择题
灰锡(以粉末状存在)和白锡(韧性很好)是锡的两种同素异形体。已知:
①Sn(s、白)+2HCl(aq)=SnCl2(aq)+H2(g) △H1
②Sn(s、灰)+2HCl(aq)=SnCl2(aq)+H2(g) △H2
③Sn(s、灰) 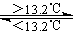 Sn(s、白) △H3=+2.1kJ·mol-1
Sn(s、白) △H3=+2.1kJ·mol-1
下列说法正确的是
A、△H1>△H2
B、锡的两种同素异形体在常温下可以相互转化,是可逆反应
C、灰锡转化为白锡的反应是吸热反应
D、锡制器皿应置于高于13.2℃的环境中,否则会自行毁坏
查看答案和解析>>
科目:高中化学 来源:2014-2015学年甘肃省武威市高一上学期期中化学试卷(解析版) 题型:填空题
在标准状况下1.7g氨气所占的体积为 ,它与同条件下 mol H2S含有相同的氢原子。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年甘肃省武威市高一上学期期中化学试卷(解析版) 题型:选择题
下列溶液中溶质的物质的量浓度为1 mol/L的是
A.将40 g NaOH溶解于1 L水中配成NaOH溶液
B.常温常压下将22.4 L HCl 气体溶于水配成1 L的盐酸溶液
C.将1 L 10 mol/L的浓盐酸与9L水混合配成溶液
D.从1000 mL 1 mol/L NaCl溶液中取出100 mL的溶液
查看答案和解析>>
科目:高中化学 来源:2014-2015学年甘肃省武威市高二上学期期中化学(理)试卷(解析版) 题型:填空题
(10分)(1)已知某溶液中只存在OH-、H+、NH4+、Cl-四种离子,某同学推测其离子浓度大小顺序有以下几种:
A.c(Cl-)>c(NH4+)>c(H+)>c(OH-)
B.c(Cl-)>c(NH4+)>c(OH-)>c(H+)
C.c(NH4+)>c(Cl-)>c(OH-)>c(H+)
D.c(Cl-)>c(H+)>c(NH4+)>c(OH-)
①上述关系一定不正确的是________(填序号)。
②若溶液中只有一种溶质,则该溶液中离子浓度的大小关系为________(填序号)。
③若四种离子浓度关系有c(NH4+)=c(Cl-),则该溶液显________(填“酸性”、“碱性”或“中性”)。
(2)常温下,有A、B、C、D四种无色溶液,它们分别是CH3COONa溶液、NH4Cl溶液、盐酸和NaNO3溶液中的一种。已知A、B的水溶液中水的电离程度相同,A、C溶液的pH相同。则:B是________溶液,C是________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年甘肃省武威市高二上学期期中化学(理)试卷(解析版) 题型:选择题
HA为酸性略强于醋酸的一元弱酸.在0.1 mol·L-1 NaA溶液中,离子浓度关系正确的是
A.c(Na+)>c(A-)>c(H+)>c(OH-) B.c(Na+)>c(OH-)>c(A-)>c(H+)
C.c(Na+)+c(H+)=c(A-)+c(OH-) D.c(Na+)+c(OH-)=c(A-)+c(H+)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省高一上学期期中化学试卷(解析版) 题型:填空题
(9分)(1)向某溶液中加入KSCN溶液无明显现象,再滴入数滴氯水后,溶液立即变成红色,则原溶液中一定含有________离子,要除去FeCl3溶液中少量的氯化亚铁,可行的办法是________(填字母)。
A.加入铜粉 B.加入铁粉 C.通入氯气 D.加入KSCN溶液
根据选用的试剂,写出除去FeCl3溶液中少量的氯化亚铁过程中发生反应的离子方程式 。
(2)电子工业常用30%的FeCl3溶液腐蚀铜箔,制造印刷线路板,写出FeCl3与金属铜反应的离子方程式 。
(3)使用过的腐蚀液会失效,但可以回收利用,某兴趣小组为了从使用过的腐蚀液中回收铜,应使用的试剂是________(填字母)。
A.铜粉 B.氯气 C.铁粉 D.KSCN溶液
(4)向沸水中逐滴滴加1 mol·L-1FeCl3溶液至液体呈透明的红褐色,该分散系中微粒直径的范围是____nm,区别该液体和FeCl3溶液可用 方法。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省高一上学期第二次阶段测试化学试卷(解析版) 题型:选择题
下列溶液中氯离子的浓度与1L 1mol/L的AlCl3溶液中氯离子物质的量浓度相等的是
A、1L 1mol/L的NaCl溶液
B、1.5L 2mol/LNH4Cl溶液
C、1L 1mol/L的AlCl3溶液和1mol/L的FeCl2混合溶液
D、2L 1.5mol/L的CaCl2溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com