
| A. | Na2O比Na2O2稳定 | B. | 均不可与水反应 | ||
| C. | 均可与CO2反应 | D. | 均是典型的碱性氧化物 |
分析 A、Na2O可与氧气继续反应生成Na2O2;
B、Na2O为碱性氧化物,与水反应只生成NaOH;
C、根据氧化钠和过氧化钠和二氧化碳反应的产物来回答;
D、碱性氧化物是指能与酸反应生成盐和水的金属氧化物;
解答 解:A.Na2O可与氧气继续反应生成Na2O2,Na2O2稳定,故A错误;
B.Na2O与水反应生成NaOH,Na2O2与水反应生成氧气和氢氧化钠,故B错误;
C.Na2O与CO2发生化合生成Na2CO3,Na2O2与CO2发生化合生成Na2CO3和氧气,则均可与CO2反应,故C正确;
D.因过氧化钠与酸反应生成盐、水和氧气,则过氧化钠不属于碱性氧化物,故D错误;
故选C.
点评 本题考查钠的重要化合物知识,为高频考点,侧重于学生的分析能力和元素化合物知识的综合理解和运用的考查,注意把握过氧化钠与水、二氧化碳反应的特点,学习中注意相关基础知识的积累,难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 0.1 mol•L-1 NaHCO3溶液与0.1 mol•L-1 NaOH溶液等体积混合,所得溶液中:c(Na+)>c(CO32-)>c(HCO32-)>c(OH-) | |
| B. | 20 mL 0.1 mol•L-1 CH3COONa溶液与10 mL 0.1 mol•L-1 HCl溶液混合后溶液呈酸性,所得溶液中:c(CH3COO-)>c(Cl-)>c(CH3COOH)>c(H+) | |
| C. | 室温下,pH=2的盐酸与pH=12的氨水等体积混合,所得溶液中:c(Cl-)+c(H+)>c(NH4+)+c(OH-) | |
| D. | 0.1 mol•L-1 CH3COOH溶液与0.1 mol•L-1 NaOH溶液等体积混合,所得溶液中:c(OH-)>c(H+)+c(CH3COOH) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
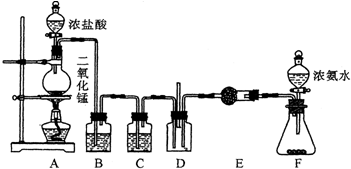
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 序号 | 电压/V | 阳极现象 | 检验阳极产物 |
| Ⅰ | x≥a | 电极附近出现黄色,有气泡产生 | 有Fe3+、有Cl2 |
| Ⅱ | a>x≥b | 电极附近出现黄色,无气泡产生 | 有Fe3+、无Cl2 |
| Ⅲ | b>x>0 | 无明显变化 | 无Fe3+、无Cl2 |
| 序号 | 电压/V | 阳极现象 | 检验阳极产物 |
| Ⅳ | a>x≥c | 无明显变化 | 有Cl2 |
| Ⅴ | c>x≥b | 无明显变化 | 无Cl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钾(K)原子基态的原子结构示意图为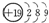 | |
| B. | Ca2+电子排布式为1s22s22p63s23p64s2 | |
| C. | 原子核内有10个中子的氧原子可表示为${\;}_{8}^{16}$O | |
| D. | H2O分子的电子式为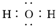 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 物质 | CH3OH | CH3OCH3 | H2O |
| t1 | 0.8 | 1.24 | 1.24 |
| t2 | 0.08 | 1.6 | 1.6 |
| A. | 平衡后升高温度,平衡常数>400 | |
| B. | t2时刻反应达到平衡状态 | |
| C. | 平衡时,反应混合物的总能量减少20kJ | |
| D. | 平衡时,再加入与起始等量的CH3OH,达新平衡后CH3OH转化率增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
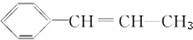 ,它可能具有的性质是( )
,它可能具有的性质是( )| A. | 易溶于水也易溶于有机溶剂 | |
| B. | 能发生加聚反应,其生成物可用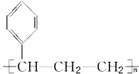 表示 表示 | |
| C. | 能使溴水褪色,但不能使酸性KMnO4溶液褪色 | |
| D. | 既能使溴水褪色,又能使酸性KMnO4溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C与浓HNO3反应 | B. | Cu与浓HNO3反应 | C. | Cu与稀HNO3反应 | D. | Mg(OH)2与HNO3反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com