
| A、1 mol NH4+ 所含质子数为10NA |
| B、10 g氖气所含原子数约为6.02×1023 |
| C、22.4 L SO2所含的分子数为NA |
| D、常温常压下,32 g O2所含原子数为2NA |


 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案科目:高中化学 来源: 题型:
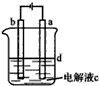 由于Fe(OH)2极易被氧化,所以实验室里很难用亚铁盐溶液与烧碱反应制的白色纯净的Fe(OH)2沉淀.应用如图所示的电解实验可制得白色纯净Fe(OH)2沉淀,两电极的材料分别为石墨和铁.下列说法正确的是( )
由于Fe(OH)2极易被氧化,所以实验室里很难用亚铁盐溶液与烧碱反应制的白色纯净的Fe(OH)2沉淀.应用如图所示的电解实验可制得白色纯净Fe(OH)2沉淀,两电极的材料分别为石墨和铁.下列说法正确的是( )| A、a电极发生的电极反应:4OH--4e-=O2↑+2H2O |
| B、为了在较短时间内看到白色沉淀,可适当加大电压 |
| C、c可以是氯化钠溶液,d可以是四氯化碳 |
| D、为了在较短时间内看到白色沉淀,可以剧烈地搅拌溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、
| ||
B、
| ||
C、
| ||
D、
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、它们的分子数之比为2:3 |
| B、它们的原子个数之比为9:8 |
| C、它们的质量之比为1:3 |
| D、同温同压下,两气体体积比为3:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氢氧化钠的摩尔质量是40g |
| B、1molNaOH的质量是40g/mol |
| C、1gH2和1gN2所含分子数相等 |
| D、阿伏伽德罗常数个钠原子的质量是23g |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、总反应为NO+NO2+O2+H2O═2HNO3 |
| B、总反应为4NO+8NO2+5O2+6H2O═12HNO3 |
| C、生成硝酸的物质的量浓度接近0.03 mol/L |
| D、生成硝酸的物质的量浓度约为0.45 mol/L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com