
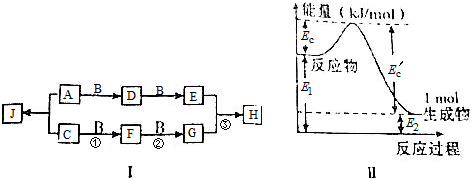
���� A��B��C�ǵ���������һ���ǽ�����һ�������壬�������ʾ��ǻ����G�ǵ���ɫ�Ĺ��壬C������B��Ӧ�õ�G������֪CΪNa��BΪO2��GΪNa2O2��F�ܺ�B��Ӧ����G����F��Na2O��
A������������Ӧ����E��A��C��Ӧ����J�����J�����ֶ�����Ԫ�ص�ԭ����Ŀ��Ϊ1��2��ͼI�����漰�ķ�Ӧ��������ǻ��Ϸ�Ӧ����AΪS��DΪSO2��EΪSO3����JΪNa2S��HΪNa2SO4���ݴ˷������
��� �⣺A��B��C�ǵ���������һ���ǽ�����һ�������壬�������ʾ��ǻ����G�ǵ���ɫ�Ĺ��壬C������B��Ӧ�õ�G������֪CΪNa��BΪO2��GΪNa2O2��F�ܺ�B��Ӧ����G����F��Na2O��
A������Ӧ����E��A��C��Ӧ����J�����J�����ֶ�����Ԫ�ص�ԭ����Ŀ��Ϊ1��2��ͼI�����漰�ķ�Ӧ��������ǻ��Ϸ�Ӧ��AΪS��DΪSO2��EΪSO3����JΪNa2S��HΪNa2SO4��
��1��J�Ļ�ѧʽΪNa2S����Ӧ�۵Ļ�ѧ����ʽΪ 2Na2O2+2SO3=2Na2SO4+O2��
�ʴ�Ϊ��Na2S��2Na2O2+2SO3=2Na2SO4+O2��
��2����Ӧ��4Na��s��+O2��g��=2 Na2O��s����H1=Q1kJ/mol��
��2Na2O��s��+O2��g��=2Na2O2��s����H2=Q2kJ/mol��
��C��B��Ӧֱ������Gʱ���Ȼ�ѧ��Ӧ����ʽ4Na��s��+2O2��g��=2Na2O2��s����H=��Q1+Q2��kJ/mol��
�ʴ�Ϊ��4Na��s��+2O2��g��=2Na2O2��s����H=��Q1+Q2��kJ/mol��
��3����Ӧ��������������������������Ϊ���ȷ�Ӧ����������¸÷�Ӧ�ķ�Ӧ�ȡ�H=-��E1-E2��kJ/mol=
-��E��c-Ec��kJ/mol��
�ʴ�Ϊ��a��b��
���� ���⿼�������ƶϣ����ʵ���ɫ�����ƶ�ͻ�ƿڣ���Ҫѧ���������ճ���������Ӧ��������ɣ��ѶȽϴ�


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��������Ӧ����㷺�����ֽ��������������գ�
��������Ӧ����㷺�����ֽ��������������գ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
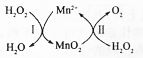 MnSO4������������������Ԫ�ط��ϵȣ��ش��������⣺
MnSO4������������������Ԫ�ط��ϵȣ��ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
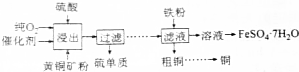
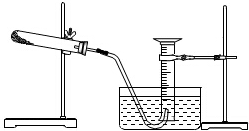 ijͬѧ����Ե���Ϊԭ����ȡ����ͭ����ʵ�飬��������ͭ������صĻ������ȡ��������������������������Իش�
ijͬѧ����Ե���Ϊԭ����ȡ����ͭ����ʵ�飬��������ͭ������صĻ������ȡ��������������������������Իش��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��NaClO��Һͨ������SO2���壺3ClO-+SO2+H2O=SO${\;}_{4}^{2-}$+Cl-+2HCl | |
| B�� | ��������Cl2ͨ��FeBr2�У�2Fe2++2Br-+2Cl2=2Fe3++4Cl-+Br2 | |
| C�� | ��̼�������Һ�μ�����������Һ��Ca2+ǡ����ȫ������Ca2++HCO3-+OH-=CaCO3��+H2O | |
| D�� | ��NH4Al��SO4��2��Һ�еμ�Ba��OH��2��Һ�����������NH4++Al3++2SO42-+2Ba2++4OH-=Al��OH��3��+2BaSO4��+NH3��H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �÷�Ӧ�ǷֽⷴӦ | B�� | �÷�Ӧ������ЧӦ�����ʱ�ЧӦ | ||
| C�� | �÷�Ӧ���ؼ���Ӧ | D�� | �÷�Ӧ�Ƿ��ȷ�Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢ڢ� | B�� | �ڢ� | C�� | �٢ڢ� | D�� | �٢ڢۢܢ� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com