
| A、Si→SiO2→H2SiO3→Na2SiO3 |
| B、Al→Al2O3→Al(OH)3→NaAlO2 |
| C、Na→NaOH→Na2CO3→NaHCO3 |
| D、Cu→CuO→Cu(OH)2→CuSO4 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、金属氧化物都是碱性氧化物 |
| B、阴离子都只有还原性,金属阳离子都只有氧化性 |
| C、元素从化合态变为游离态时,一定失去电子,发生氧化反应 |
| D、人工固氮和漂白粉使石蕊溶液褪色都发生了氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

 经两步反应制得,写出第一步反应的化学方程式
经两步反应制得,写出第一步反应的化学方程式查看答案和解析>>
科目:高中化学 来源: 题型:
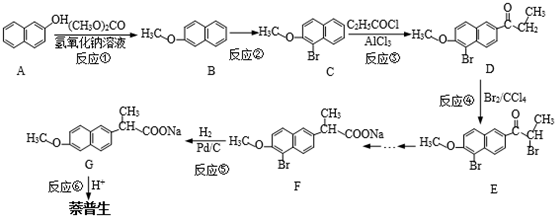
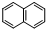 )的化学性质与苯相似.
)的化学性质与苯相似. )外,最有可能生成的副产物(与H互为同分异构体)的结构简式是
)外,最有可能生成的副产物(与H互为同分异构体)的结构简式是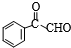 的合成路线流程图(无机试剂任用).
的合成路线流程图(无机试剂任用).| O2 |
| 催化剂 |
| Na |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、O和F无正化合价 |
| B、1mol O2参加反应,转移1mol e- |
| C、上述反应中O2作氧化剂 |
| D、上述反应属于加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Al3+、Fe3+、Br-、SO42- |
| B、K+、Ca2+、SO42-、Cl- |
| C、H+、Cu2+、I-、NO3- |
| D、Al3+、Mg2+、NO3-、HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com