
| A、NH4Cl |
| B、NH4HCO3 |
| C、NH4HSO4 |
| D、(NH4)2SO4 |


 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案科目:高中化学 来源: 题型:
| A、原子组成一样 |
| B、O-H键的化学键类型一样 |
| C、羟基中氢原子活性性不同 |
| D、酚羟基能发生电离,醇羟基也能发生电离 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、溶液中析出0.05mol Cu |
| B、溶液中析出0.1mol Ag |
| C、溶液中Cu2+与Fe2+的浓度之比为1:2 |
| D、往反应后的溶液中再加入0.1mol 铁粉,铁粉恰好完全溶解 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 (1)将下列离子Na+、K+、Cu2+、H+、NO3-、Cl-、CO32-、OH-,按可能大量共存于同一溶液的情况,则分成A、B两组,而且每组中均含两种阳离子和两种阴离子,则A组
(1)将下列离子Na+、K+、Cu2+、H+、NO3-、Cl-、CO32-、OH-,按可能大量共存于同一溶液的情况,则分成A、B两组,而且每组中均含两种阳离子和两种阴离子,则A组查看答案和解析>>
科目:高中化学 来源: 题型:
| A、pH=1的NaHSO4溶液:c(H+)=c(SO42-)+c(OH-) |
| B、含有AgCl和AgI固体的悬浊液:c(Ag+)>c(Cl-)=c(I-) |
| C、0.1 mol/L NH4Cl与0.1 mol/L氨水等体积混合(pH>7):c(NH3?H2O)>c(NH4+)>c(Cl-)>c(OH-) |
| D、含等物质的量的NaHC2O4和Na2C2O4的溶液:3c(Na+)=2[c(HC2O4-)+c(C2O42-)+c(H2C2O4)] |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、聚丙烯的链节:-CH2-CH2-CH2- | ||
B、NH4Cl的电子式: | ||
C、F-结构示意图: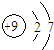 | ||
D、中子数为20的氯原子:
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com