
| A. | 纯净物都是由同种分子构成 | |
| B. | 纯净物可能是单质,也可能是化合物 | |
| C. | 矿泉水是纯净物 | |
| D. | 纯净物就是由同种元素组成的物质 |
分析 物质分为混合物和纯净物,混合物是由两种或两种以上的物质组成;纯净物是由一种物质组成.纯净物又分为单质和化合物.由同种元素组成的纯净物叫单质;由两种或两种以上的元素组成的纯净物叫化合物.
解答 解:A.纯净物是由一种物质组成,可以是由离子组成,故A错误;
B.纯净物是由一种物质组成,纯净物又分为单质和化合物,由同种元素组成的纯净物叫单质;由两种或两种以上的元素组成的纯净物叫化合物,故B正确;
C.矿泉水含多种物质,是混合物,故C错误;
D.纯净物是由一种物质组成,可以是化合物,故D错误.
故选B.
点评 本考点考查了物质的分类,要加强记忆混合物、纯净物、单质、化合物、氧化物等基本概念,并能够区分应用.本考点的基础性比较强,主要出现在选择题和填空题中.


科目:高中化学 来源: 题型:解答题
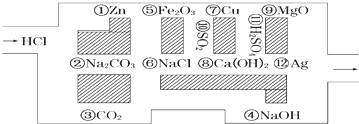
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原混合溶液中c(Na+)=0.2 mol•L-1 | |
| B. | 电解后溶液中c(H+)=0.4mol•L-1 | |
| C. | 上述电解过程中共转移0.4 mol电子 | |
| D. | 电解后得到的Cu的物质的量为0.05mol |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
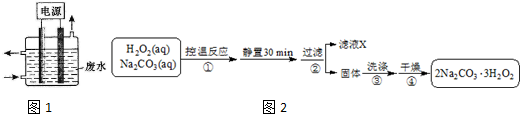
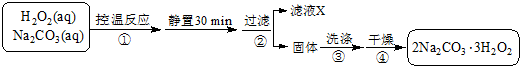
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在pH=12的溶液中:K+、Cl-、HCO3-、Na+ | |
| B. | 在[H+]=10-12 mol•L-1的溶液:K+、Ba2+、Cl-、Br- | |
| C. | 使酚酞试液变红的溶液:Na+、Cl-、SO42-、Fe3+ | |
| D. | 使石蕊试液变红的溶液:K+、MnO4-、I-、H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
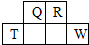 短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T的单质既可与盐酸反应,又可与NaOH溶液反应,请回答下列问题:
短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T的单质既可与盐酸反应,又可与NaOH溶液反应,请回答下列问题: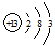 .
.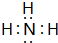
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
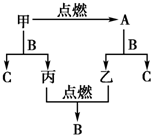 A、B、C是三种常见的化合物,A为淡黄色固体.它们之间的转化关系如图所示.
A、B、C是三种常见的化合物,A为淡黄色固体.它们之间的转化关系如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com