
【题目】实验室用下图所示装置制备干燥纯净的氯气,并进行氯气的性质实验,请回答下列问题:
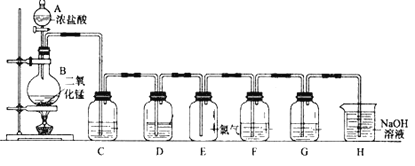
(1)仪器A的名称是____________。
(2)烧瓶中发生反应的化学方程式为(含条件)________________________。
(3)为在E装置中收集到干燥纯净的氯气,装置C中盛放的试剂为_____________(填写名称),作用是____________________________。
(4)F处盛有Na2S溶液,可用置换反应的原理证明氯的非金属性强于硫。反应的离子方程式为 _________________________________________。
(5)G中加入的是淀粉碘化钾溶液,发生反应的现象为_____________________________________。
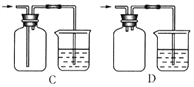
(6)H为尾气处理装置,写出该装置中的离子方程式_________________________。有人认为,用NaOH溶液吸收尾气,可能会引起倒吸。下列装置中,能起到防倒吸作用的是_______(填序号字母)。

【答案】 分液漏斗 MnO2+4HCl(浓)![]() MnCl2+2H2O+Cl2↑ 饱和食盐水(饱和氯化钠溶液) 除去氯气中的氯化氢 Cl2+S2- = 2Cl-+S↓ 溶液变蓝 Cl2+2OH- = Cl-+ClO-+H2O BD
MnCl2+2H2O+Cl2↑ 饱和食盐水(饱和氯化钠溶液) 除去氯气中的氯化氢 Cl2+S2- = 2Cl-+S↓ 溶液变蓝 Cl2+2OH- = Cl-+ClO-+H2O BD
【解析】(1)根据流程图,仪器A为分液漏斗,故答案为:分液漏斗;
(2)烧瓶中浓盐酸与二氧化锰在加热条件下反应生成氯气,反应的化学方程式为MnO2+4HCl(浓)![]() MnCl2+2H2O+Cl2↑,故答案为:MnO2+4HCl(浓)
MnCl2+2H2O+Cl2↑,故答案为:MnO2+4HCl(浓)![]() MnCl2+2H2O+Cl2↑;
MnCl2+2H2O+Cl2↑;
(3)生成的氯气中混有氯化氢和水蒸气,为在E装置中收集到干燥纯净的氯气,装置C中盛放的试剂为饱和食盐水,作用是除去氯气中的氯化氢,故答案为:饱和食盐水;除去氯气中的氯化氢;
(4)F处盛有Na2S溶液,氯气与硫化钠溶液反应生成硫单质沉淀,反应的离子方程式为Cl2+S2- = 2Cl-+S↓,故答案为:Cl2+S2- = 2Cl-+S↓;
(5)G中加入的是淀粉碘化钾溶液,氯气与碘化钾反应生成碘单质,碘遇到淀粉变蓝色,故答案为:溶液变蓝;
(6)H为尾气处理装置,氢氧化钠溶液与氯气反应生成氯化钠和次氯酸钠,反应的离子方程式为Cl2+2OH- = Cl-+ClO-+H2O。B中倒扣的漏斗可以防止倒吸,D在的安全瓶可以防止倒吸,为了防止引起倒吸,可以选用BD装置,故答案为:Cl2+2OH- = Cl-+ClO-+H2O;BD。


科目:高中化学 来源: 题型:
【题目】氯元素在自然界有35Cl和37Cl两种同位素,在计算式34.969×75.77%+36.966×24.23% =35.453中,说法不正确的是
A.75.77%表示35Cl的质量分数B.24.23%表示37Cl的丰度
C.35. 453表示氯元素的相对原子质量D.36.966表示37Cl的相对原子质量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一小块金属钠长期露置于空气中发生一系列变化,最终产物是( )
A. NaOH B. Na2CO3 C. Na2CO3·10H2O D. Na2O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向100g浓度为18mol/L的浓硫酸(密度为ρg/cm3)中加入一定量的水,稀释成9mol/L的硫酸,则加入水的体积为
A.小于100mLB.等于100mLC.大于100mLD.等于100/ρmL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质按酸、碱、盐分类顺次排列的是( )
A. 硫酸(H2SO4)、纯碱(Na2CO3)、食盐(NaCl)
B. 硝酸(HNO3)、烧碱(NaOH)、胆矾(CuSO45H2O)
C. 醋酸(CH3COOH)、乙醇(C2H5OH)、硫酸铵[(NH4)2SO4]
D. 盐酸(HCl)、熟石灰[Ca(OH)2]、苛性钠(NaOH)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于阿司匹林,下列说法正确的是( ) 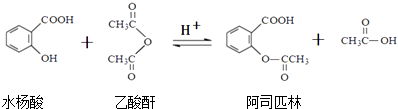
A.不能用FeCl3 溶液鉴别水杨酸和阿司匹林
B.服用阿司匹林出现水杨酸反应时,可静脉注射NaHCO3溶液
C.1 mol阿司匹林最多可消耗2 mol NaOH
D.该反应不属于取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氰化物在冶金等行业应用广泛,含氰废水的处理显得尤为重要.含氰废水中的氰化物常以[Fe(CN)6]3﹣和CN﹣的形式存在,工业上有多种废水处理方法. 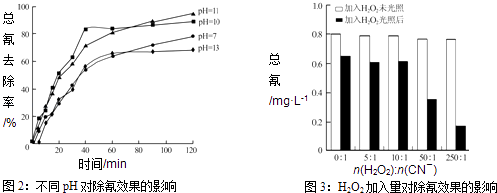
(1)电解处理法 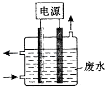
图1电源废水铁电极石墨电极
用图1所示装置处理含CN﹣废水时,控制溶液pH为9~10并加入NaCl,一定条件下电解,阳极产生的ClO﹣将CN﹣氧化为无害物质而除去.铁电极为(填“阴极”或“阳极”),阳极产生ClO﹣的电极反应为 .
(2)UV(紫外光线的简称)﹣H2O2氧化法. 实验过程:取一定量含氰废水,调节pH,加入一定物质的量的H2O2 , 置于UV工艺装置中,光照一定时间后取样分析.
【查阅资料】①在强碱性溶液中4[Fe(CN)6]3﹣+4OH﹣═4[Fe(CN)6]4﹣+O2↑+2H2O,[Fe(CN)6]4﹣更稳定;
②[Fe(CN)6]3﹣转化为CN﹣容易被H2O2除去;
③HCN是有毒的弱酸,易挥发.
Ⅰ.废水中的CN一经以下反应实现转化:CN一+H2O2+H2O═A+NH3↑,则A是(用符号表示).
Ⅱ.K3[Fe(CN)6]在中性溶液中有微弱水解,用方程式表示水解反应 .
Ⅲ.含氰废水在不同pH下的除氰效果如图2所示,pH选择的最佳范围应为(a.7﹣10;b.10﹣11;c.11﹣13),解释选择该pH范围的原因 .
Ⅳ.图3表示某pH时,加入不同量H2O2 , 处理30min后测定的样品含氰浓度.由图可知:n(H2O2):n(CN﹣)=250:1时,剩余总氰为0.16mgL﹣1 , 除氰率达80%,计算0﹣30min时间段反应速率v(CN﹣)=mgL﹣1min﹣1(结果保留两位有效数字).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com