
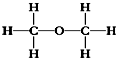
 央视3•15曝光,在液化石油气中掺混二甲醚的事件.二甲醚(常压下沸点-24.9℃)是一种可溶于水的化工原料,常被用作一些燃料的替代品,其结构式如下.下列有关二甲醚的叙述中正确的是( )
央视3•15曝光,在液化石油气中掺混二甲醚的事件.二甲醚(常压下沸点-24.9℃)是一种可溶于水的化工原料,常被用作一些燃料的替代品,其结构式如下.下列有关二甲醚的叙述中正确的是( )| A. | 二甲醚和乙醇互为同分异构体且和甲醇互为同系物 | |
| B. | 二甲醚是一种有机物,属于非电解质 | |
| C. | 标准状况下,燃烧11.2L二甲醚一定生成22.4LCO2 | |
| D. | 4.6g该物质中含有共价键的数目为7×6.02×1022 |
分析 A.分子式相同结构不同的有机物互为同分异构体;结构相似,在分子组成上相差一个或n个-CH2原子团的有机物互称同系物;
B.在水溶液里和熔融状态下不导电的化合物是非电解质;
C.标况下,二甲醚是液体,气体摩尔体积不适用于液体和固体;
D.一个二甲醚分子中含有共价键数目是8个,4.6g二甲醚的物质的量为$\frac{4.6g}{46g/mol}$=0.1mol.
解答 解:A.分子式相同结构不同的有机物互为同分异构体,所以二甲醚和乙醇是同分异构体;结构相似,在分子组成上相差一个或n个-CH2原子团的有机物互称同系物,但和甲醇不属于同系物,故A错误;
B.在水溶液里和熔融状态下不导电的化合物是非电解质,二甲醚是有机物,不溶于水,在水中以分子存在,所以属于非电解质,故B正确;
C.标况下,二甲醚是液体,气体摩尔体积不适用于液体和固体,所以无法计算,故C错误;
D.一个二甲醚分子中含有共价键数目是8个,4.6g二甲醚的物质的量为$\frac{4.6g}{46g/mol}$=0.1mol,则4.6g该物质中含有共价键的数目为8×6.02×1022,故D错误.
故选B.
点评 本题考查有机物结构和性质,涉及同系物、同分异构体、非电解质等基本概念,熟悉概念内涵是解本题关键,同分异构体的书写或同分异构体种类的判断是高考高频点,易错选项是C.


 综合自测系列答案
综合自测系列答案科目:高中化学 来源: 题型:选择题
| 选项 | 反应 | 铝 | 镁 |
| A | 与非金属 | 能被Cl2、O2氧化 | 能与N2、O2反应 |
| B | 与水 | 能与沸水反应 | 反应很困难 |
| C | 与碱 | 能溶于强碱溶液 | 不反应 |
| D | 与某些氧化物 | 能与Fe2O3、MnO2、Cr2O3等 金属氧化物发生铝热反应 | 能在CO2中燃烧 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在1mol甲基(-CH3)中,电子总数9NA | |
| B. | 在1mol的Na2O2中,有2NA个阴离子 | |
| C. | 标准状况下,22.4L CHC13所含有的分子数目为NA | |
| D. | Cu、A1为电极,浓硝酸为电解质溶液所构成的原电池中,导线上流过NA个电子,则A1电极放出气体的体积一定为22.4L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在H202分解中加入MnO2 | |
| B. | Zn与25%的稀硫酸反应制取H2时,改用98%的浓硫酸 | |
| C. | 在NaOH与HCL两溶液反应时,增大压强 | |
| D. | Na与水反应时增大水的用量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 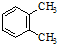 与 与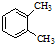 是同分异构体 是同分异构体 | |
| B. | 苯可以发生加成反应 | |
| C. | 可通过萃取的方法,从煤中提取苯 | |
| D. | 向2mL苯中加入1mL酸性高锰酸钾溶液,震荡后静置,可观察到液体分层,上层呈紫红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com