
| A. | 1:8 | B. | 8:1 | C. | 1:5 | D. | 5:1 |
 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:高中化学 来源: 题型:选择题
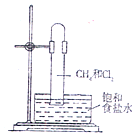 取一支硬质大试管,通过排饱和食盐水的方法先后收集半试管甲烷和半试管氯气(如图),下列对于试管内发生的反应及现象的说法正确的是( )
取一支硬质大试管,通过排饱和食盐水的方法先后收集半试管甲烷和半试管氯气(如图),下列对于试管内发生的反应及现象的说法正确的是( )| A. | 此反应无光照也可发生 | |
| B. | 甲烷和Cl2反应后的产物只有CH3Cl和HCl | |
| C. | 盛放饱和食盐水的水槽底部会有少量晶体析出 | |
| D. | CH4和Cl2完全反应后液面上升,液体充满试管 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 正常雨水PH等于7,酸雨的PH小于7 | |
| B. | 金属钠着火燃烧时,可用泡沫灭火器灭火 | |
| C. | 在放电条件下,氮气和氧气化合生成二氧化氮 | |
| D. | 冷的浓硫酸与铁、铝反应时会使金属表面生成致密的氧化物而钝化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 18 g D2O和18 g H2O中含有的质子数均为10NA | |
| B. | 1 mol Cu和2mol热的浓硫酸反应可生成NA个SO2分子 | |
| C. | 3 mol单质Fe完全转变为Fe3O4,失去8NA个电子 | |
| D. | 标准状况下,22.4 L N2和H2混合气中含NA个原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HNO3作氧化剂 | |
| B. | 氧化剂和还原剂的物质的量之比为1:1 | |
| C. | 当生成1molI2时,转移2mol电子 | |
| D. | 由该反应可知还原性:Se>KI |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
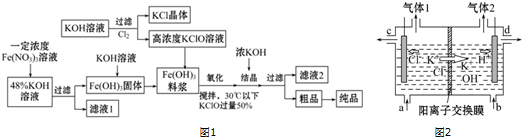
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 0.20 | B. | 0.16 | C. | 0.12 | D. | 0.10 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 裂化汽油不能萃取溴水中的溴 | |
| B. | 石油的分馏以及煤的气化和液化是物理变化 | |
| C. | 煤中含有大量的苯等芳香烃,煤是芳香烃的主要来源 | |
| D. | 煤属于有机化合物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com