
| A. | 氯仿 | B. | 溴苯 | C. | 2-氯-2-甲基丙烷 | D. | 乙醇 |
分析 与-X或羟基相连碳原子相邻的碳原子上有氢原子的卤代烃和醇能发生消去反应;所有卤代烃和酯均能发生水解反应,以此解答该题.
解答 解:A.氯仿可发生水解反应,因只含有1个C原子,则不能发生消去反应,故A错误;
B.溴苯含有苯环,性质稳定,不能发生消去反应,故B错误;
C.2-氯-2-甲基丙烷与Cl原子相连碳原子的相邻碳上有氢原子,能发生消去反应,也能在氢氧化钠的水溶液中发生水解反应,故C正确;
D.乙醇不能发生水解反应,故D错误.
故选C.
点评 本题考查有机物的结构和性质,侧重于卤代烃的水解反应、消去反应的考查,难度不大,注意卤代烃发生消去反应的结构特点是:只有-X相连碳原子的相邻碳上有氢原子的才能发生消去反应.


 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案科目:高中化学 来源: 题型:推断题
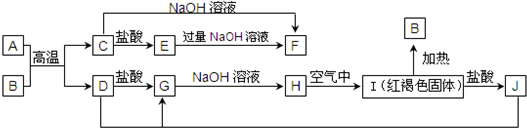
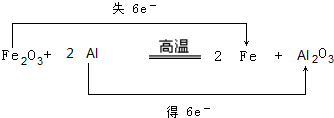 .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| t/s | 0 | 50 | 150 | 250 | 350 |
| n(PCl3)/mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
| A. | 反应在前50s的平均速率v(Cl2)=0.0016 mol•L-1•min-1 | |
| B. | 保持其他条件不变,升高温度,平衡时c(PCl3)=0.11 mol•L-1,则该反应的△H<0 | |
| C. | 温度为T时,起始时向容器中充入1.0 mol PCl5、0.20 mol PCl3和0.20 mol Cl2,反应达到平衡前v(正)>v(逆) | |
| D. | 温度为T时,起始时向容器中充入0.5 mol PCl3和0.5 mol Cl2,达到平衡时,PCl3的转化率小于80% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2通入盐酸酸化的硝酸钡溶液 | B. | 在AlCl3溶液中滴入过量的氨水 | ||
| C. | 在空气中长期存放的漂白粉溶液 | D. | 将少量NaAlO2投入盐酸中 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 ,新戊烷的结构简式为C(CH3)4.
,新戊烷的结构简式为C(CH3)4.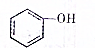 (填“>”、“<”或“=”,下同)
(填“>”、“<”或“=”,下同)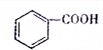 (提示:类比醇与酚的酸性)
(提示:类比醇与酚的酸性) .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
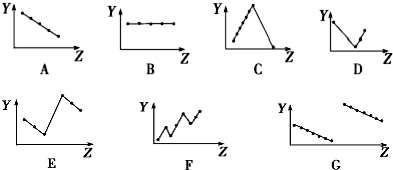
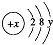
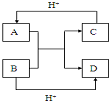
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2项 | B. | 3项 | C. | 4项 | D. | 5项 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题


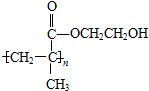 .
.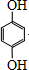 .
.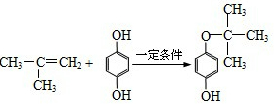 ,反应类型是加成反应.
,反应类型是加成反应.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 产生气体的质量为0.3g | |
| B. | 合金中镁与铝的物质的量之比为1:2 | |
| C. | 溶液X中剩余NaOH的物质的量为0.2 mol | |
| D. | 向溶液X中通入足量C02,过滤,将沉淀充分灼烧得固体15.6 g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com