
硼、镁及其化合物在工农业生产中应用广泛。
已知:硼镁矿主要成分为Mg2B2O5?H2O,硼砂的化学式为Na2B4O7?10H2O。利用硼镁矿制取金属镁及粗硼的工艺流程为:
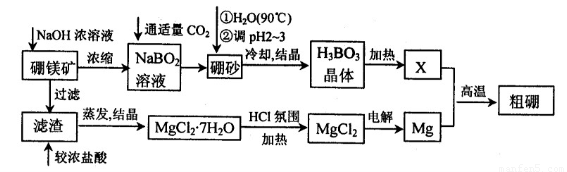
回答下列有关问题:
(1)硼砂中B的化合价为???????? ,溶于热水后,常用H2SO4调pH2~3制取H3BO3,反应的离子方程式为????????????? 。X为H3BO3晶体加热脱水的产物,其与Mg制取粗硼的化学方程式为??????????????? 。
(2)MgCl2·7H2O需要在HCl氛围中加热,其目的是????????????????????????? ? 。若用惰性电极电解MgCl2溶液,其阴极反应式为 ??????????????? 。
(3)镁-H2O2酸性燃料电池的反应机理为Mg+H2O2+2H+==Mg2++2H2O,则正极反应式为????????????????? 。若起始电解质溶液pH=1,则pH=2时溶液中Mg2+离子浓度为?????? 。已知Ksp[Mg(OH)2]=5.6 10-12,当溶液pH=6时?????? (填“有”或“没有”)Mg(OH)2沉淀析出。
10-12,当溶液pH=6时?????? (填“有”或“没有”)Mg(OH)2沉淀析出。
(4)制得的粗硼在一定条件下生成BI3,BI3加热分解可以得到纯净的单质硼。现将??? 0.020g粗硼制成的BI3完全分解,生成的I2用0.30mol·L-1 Na2S2O3(H2S2O3为弱酸)溶液滴定至终点,消耗Na2S2O3溶液18.00mL。盛装Na2S2O3溶液的仪器应为??????? 滴定管(填“酸式”或“碱式”)。该粗硼样品的纯度为 ???? 。(提示:I2+2S2O32-=2I-+S4O62-)
(1)+3(2分) B4O72-+2H++5H2O= 4H3BO3(2分)Mg+B2O3===2B+3MgO(2分)?
(2)防止MgCl2水解生成Mg(OH)2(2分)?
2H2O+Mg2++2e-= H2↑+Mg(OH)2↓(2分)
(3)H2O2+2H++2e-=2H2O(2分)??? 0.045 mol·L-1(2分)? 没有(2分)
(4)碱式(2分)? 99%(2分)
【解析】
试题分析:(1)根据硼砂的化学式Na2B4O7?10H2O和化合价的代数和为0,可得B的化合价为+3;B4O72-与2H+反应可得H3BO3,离子方程式为:B4O72-+2H++5H2O= 4H3BO3;X为H3BO3晶体加热脱水的产物,为B2O3,与Mg发生氧化还原反应,化学方程式为:Mg+B2O3===2B+3MgO。
(2)MgCl2为强酸弱碱盐,能发生水解反应,所以MgCl2·7H2O在HCl氛围中加热的目的是:防止MgCl2水解生成Mg(OH)2;用惰性电极电解MgCl2溶液,阴极反应为H2O电离出的H+放电,电解方程式为:2H2O+Mg2++2e-= H2↑+Mg(OH)2↓
(3)镁-H2O2酸性燃料电池的正极为H2O2放电,电极方程式为:H2O2+2H++2e-=2H2O;起始电解质溶液pH=1,pH=2时反应的H+为:0.1mol?L?1—0.01mol?L?1=0.09mol?L?1,根据Mg+H2O2+2H+==Mg2++2H2O,可得Mg2+离子浓度为0.045 mol·L-1;溶液pH=6时,c(OH?)=10-8mol?L?1,Q [Mg(OH)2]= 0.045 mol·L-1×[10-8mol?L?1]2=4.5×10-18 < Ksp[Mg(OH)2],所以没有Mg(OH)2沉淀析出。
(4)Na2S2O3为强碱弱酸盐,水解显碱性,所以Na2S2O3溶液应盛放在碱式滴定管内;根据元素守恒和离子方程式可得:2B ~ 2BI3 ~ 3I2 ~ 6 S2O32-,所以粗硼样品的纯度为:0.018L×0.30mol?L?1 ×1/3×11g/mol÷×100% = 99%
考点:本题考查化学工艺流程的分析、化学方程式、离子方程式和电解方程式的书写、盐类的水解、原电池和电解池原理、滴定管的使用、化学计算。


科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
(14分)镁及其化合物在生产生活中有重要的作用。以水氯镁石(主要成分为MgCl2·6H2O)为原料生产碱式碳酸镁的主要流程如下:
(1)上述流程中的滤液浓缩结晶,所得主要固体物质的化学式为 。指出该物质在工农业生产中的一种用途: 。
(2)写出预氨化时发生的主要反应的离子方程式: 。
(3)沉淀镁时反应的温度不宜过高,原因是 。
(4)设计一个实验,确定产品碱式碳酸镁aMgCO3·bMg(OH)2·cH2O中a、b、c的值,请完善下列实验步骤(可用试剂:浓硫酸、碱石灰):
①样品称量;②高温分解;③ ;④ ;⑤称量MgO。
18.2g产品完全分解后,产生6.6g CO2和8.0g MgO,由此可知,产品的化学式中:
a= ;b = ;c = 。
(5)从水氯镁石中可以提取无水氯化镁,电解熔融态的无水氯化镁可以得到金属镁。有同学认为:电解熔融的MgO也可制金属镁,在实际生产中可简化生产步骤,体现生产的简约性和经济性原则。你同意该同学的想法吗?为什么?你的观点是 。理由是 。
查看答案和解析>>
科目:高中化学 来源:2011届安徽省宣城市高三第二次调研测试(理综)化学部分 题型:填空题
(14分)镁及其化合物在生产生活中有重要的作用。以水氯镁石(主要成分为MgCl2·6H2O)为原料生产碱式碳酸镁的主要流程如下: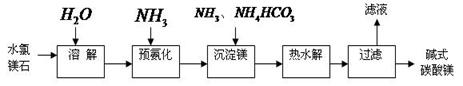
(1)上述流程中的滤液浓缩结晶,所得主要固体物质的化学式为 。指出该物质在工农业生产中的一种用途: 。
(2)写出预氨化时发生的主要反应的离子方程式: 。
(3)沉淀镁时反应的温度不宜过高,原因是 。
(4)设计一个实验,确定产品碱式碳酸镁aMgCO3·bMg(OH)2·cH2O中a、b、c的值,请完善下列实验步骤(可用试剂:浓硫酸、碱石灰):
①样品称量;②高温分解;③ ;④ ;⑤称量MgO。
18.2g产品完全分解后,产生6.6g CO2和8.0g MgO,由此可知,产品的化学式中:
a= ;b = ;c = 。
(5)从水氯镁石中可以提取无水氯化镁,电解熔融态的无水氯化镁可以得到金属镁。有同学认为:电解熔融的MgO也可制金属镁,在实际生产中可简化生产步骤,体现生产的简约性和经济性原则。你同意该同学的想法吗?为什么?你的观点是 。理由是 。
查看答案和解析>>
科目:高中化学 来源:2010-2011学年安徽省宣城市高三第二次调研测试(理综)化学部分 题型:填空题
(14分)镁及其化合物在生产生活中有重要的作用。以水氯镁石(主要成分为MgCl2·6H2O)为原料生产碱式碳酸镁的主要流程如下:
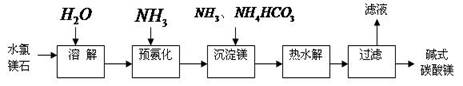
(1)上述流程中的滤液浓缩结晶,所得主要固体物质的化学式为 。指出该物质在工农业生产中的一种用途: 。
(2)写出预氨化时发生的主要反应的离子方程式: 。
(3)沉淀镁时反应的温度不宜过高,原因是 。
(4)设计一个实验,确定产品碱式碳酸镁aMgCO3·bMg(OH)2·cH2O中a、b、c的值,请完善下列实验步骤(可用试剂:浓硫酸、碱石灰):
①样品称量;②高温分解;③ ;④ ;⑤称量MgO。
18.2g产品完全分解后,产生6.6g CO2和8.0g MgO,由此可知,产品的化学式中:
a= ;b = ;c = 。
(5)从水氯镁石中可以提取无水氯化镁,电解熔融态的无水氯化镁可以得到金属镁。有同学认为:电解熔融的MgO也可制金属镁,在实际生产中可简化生产步骤,体现生产的简约性和经济性原则。你同意该同学的想法吗?为什么?你的观点是 。理由是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com