
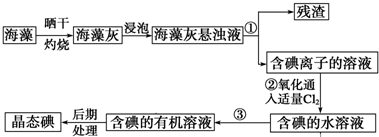
分析 海带晒干灼烧可生成水和二氧化碳,海带灰中含有碘化钾等物质,溶于水,浸泡过滤得到含有碘离子的溶液,通入氯气,氯气置换出碘,得到碘的水溶液,用有机溶剂萃取得到含碘的有机溶液,经蒸馏可得到碘,以此解答该题.
(1)海带灼烧成灰,浸泡溶解得到海带灰悬浊液,分离固体和液体用过滤;
(2)根据实验操作步骤①为灼烧来分析用到的实验仪器,灼烧海带时,所用到的仪器除需要泥三角除酒精灯和泥三角外,还需要坩埚盛放海带,;
(3)萃取的基本原则两种溶剂互不相溶,且溶质在一种溶剂中的溶解度比在另一种大的多,据此来选择合适的试剂.
解答 解:(1)①海带晒干灼烧可生成水和二氧化碳,海带灰中含有碘化钾等物质溶于水,残渣不溶于水,浸泡溶解得到海带灰悬浊液,分离固体和液体用过滤,
故答案为:过滤;
(2)灼烧固体物质一般使用(瓷)坩埚,而坩埚加热需要用泥三脚支撑然后放在三脚架上,三脚架下面的空间放酒精灯,
故答案为:C;
(3)萃取的基本原则两种溶剂互不相溶,且溶质在一种溶剂中的溶解度比在另一种大的多,故可用四氯化碳,酒精、甘油、乙酸等和水是互溶的,不能选择,
故答案为:B.
点评 本题考查物质的分离和提纯,学习中注意掌握过滤、萃取、蒸馏等操作,属于实验综合知识的考查,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A | B | C | D | |
| 强电解质 | C | NaCl | CaCO3 | HNO3 |
| 弱电解质 | CH3COOH | NH3 | HCl | H2O |
| 非电解质 | 蔗糖 | BaSO4 | C2H5OH | 酒精 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 13.6g | B. | 10.2g | C. | 6.8g | D. | 1.7g |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 操 作 | 现 象 |
| 关闭弹簧夹,滴加一定量浓硫酸,加热 | A中有白雾生成,铜片表面产生气泡 B中有气泡冒出,产生大量白色沉淀 C 中产生白色沉淀,液面上方略显浅棕色并逐渐消失 |
| 打开弹簧夹,通入N2,停止加热,一段时间后关闭 | |
| 从B、C中分别取少量白色沉淀,加稀盐酸 | 均未发现白色沉淀溶解 |
| 甲 | 大量白色沉淀 |
| 乙 | 少量白色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 需用托盘天平称取NaOH固体19.6g | |
| B. | 氢氧化钠固体溶解之后迅速转移至容量瓶中,以防变质 | |
| C. | 加蒸馏水至离刻度线1~2cm时改用胶头滴管定容 | |
| D. | 容量瓶使用前没有干燥会使所配溶液浓度偏低 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe(OH)3胶体无色、透明,能产生丁达尔效应 | |
| B. | 硫酸溶液的导电性一定比醋酸溶液的导电性强 | |
| C. | 用萃取分液的方法除去酒精中的水 | |
| D. | SO3溶于水后得到的溶液可以导电,但SO3是非电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com