
 习题精选系列答案
习题精选系列答案科目:高中化学 来源: 题型:
25 ℃时,下列说法正确的是双选) )。
A.pH=12的NaOH溶液中,cH+)=10-12 mol·L-1,将溶液稀释为原体积的10倍后cH+)=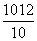 mol·L-1=10-13mol·L-1
mol·L-1=10-13mol·L-1
B.pH=3的CH3COOH溶液与pH=11的NaOH溶液等体积混合后,因生成的CH3COONa
水解,所以由水电离出的cH+)<10-7mol·L-1
C.pH=2的盐酸、pH=2的醋酸中由水电离出的cH+)均为10-12 mol·L-1
D.pH=11和pH=13的NaOH溶液等体积混合后,溶液中的cH+)=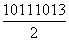 mol·L-1
mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数的值。下列叙述正确的是( )
A.在标况下,11.2 L NO与11.2 L O2混合后所含分子数为0.75NA
B.常温常压下,16 g O3所含的电子数为8NA
C.0.1 mol Na2O2晶体中含有0.4NA个离子
D.铝跟氢氧化钠溶液反应生成1 mol氢气时,转移的电子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
有机物A~H均含苯环,它们之间的转化关系如下。已知:B与FeCl3溶液混合无颜色变化。
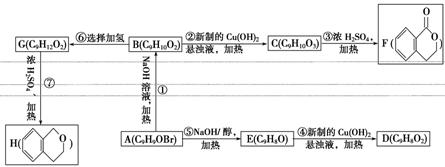
回答下列问题:
(1)B的结构简式为________。
(2)①~⑦中属于取代反应的是________(填序号)。
(3)写出一种可鉴别D、F的试剂:________。
(4)写出反应⑦的化学方程式:______________________________________________。
(5)写出同时符合下列条件的C的同分异构体的结构简式:________________________
________________________________________________。
①化合物是1,3,5三取代苯
②苯环上的三个取代基中分别含有醇羟基、酚羟基和醛基
查看答案和解析>>
科目:高中化学 来源: 题型:
已知元素X的电负性数值为2.5,元素Y的电负性数值是3.5,元素Z的电负性数值为1.2,元素W的电负性数值为2.4。你认为上述四种元素中,哪两种最容易形成离子化合物
A.X与Y B.X与W C.Y与Z D.Y与W
查看答案和解析>>
科目:高中化学 来源: 题型:
能说明BF3分子中的4个原子处于同一平面的理由是( )
A.3个B—F的键能相同 B.3个B—F的键长相同
C.3个B—F的键角均为120° D.3个B—F的键均为σ键
查看答案和解析>>
科目:高中化学 来源: 题型:
不能用化学平衡移动原理说明的事实是( )
A.合成氨在高压下进行是有利的
B.温度过高对合成氨不利
C.使用催化剂能使合成氨速率加快
D.及时分离从合成塔中出来的混合气,有利于合成氨
查看答案和解析>>
科目:高中化学 来源: 题型:

某研究小组为探究弱酸性条件下铁发生电化学腐蚀类型的影响因素,将混合均匀的新制铁粉和碳粉置于锥形瓶底部,塞上瓶塞(如图1)。从胶头滴管中滴入几滴醋酸溶液,同时测量容器中的压强变化。
(1)请完成以下实验设计表(表中不要留空格):
| 编号 | 实验目的 | 碳粉/g | 铁粉/g | 醋酸/% |
| ① | 为以下实验作参照 | 0.5 | 2.0 | 90.0 |
| ② | 醋酸浓度的影响 | 0.5 | 36.0 | |
| ③ | 0.2 | 2.0 | 90.0 |
(2)编号①实验测得容器中压强随时间变化如图2。t2时,容器中压强明显小于起始压强,其原因是铁发生了________腐蚀,请在图3中用箭头标出发生该腐蚀时电子流动方向;此时,碳粉表面发生了________(填“氧化”或“还原”)反应,其电极反应式是______________________________。

(3)该小组对图2中0~t1时压强变大的原因提出了如下假设,请你完成假设二:
假设一:发生析氢腐蚀产生了气体;
假设二:________________________________________________________________________;
……
(4)为验证假设一,某同学设计了检验收集的气体中是否含有H2的方案。请你再设计一个实验方案验证假设一,写出实验步骤和结论。
| 实验步骤和结论(不要求写具体操作过程): |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com