
【题目】下列各组物质属于同位素的是___________,属于同分异构体的是_________,属于同一物质的是__________。
(1)O2和O3
(2)3517Cl和3717Cl
(3)CH3CH3和CH3CH2CH2CH3
(4)金刚石和石墨
(5)氕、氘、氚
(6)CH3CH2CH2CH(CH3)CH2CH3和CH3CH2CH(CH3)CH(CH3)CH3
(7)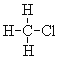 和
和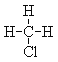
【答案】 (2 )(5) (6) (7)
【解析】(1)O2和O3 均为氧元素组成的不同单质,互为同素异形体;(2)3517Cl和3717Cl的核电荷数相同,中子数不等,互为同位素;(3)CH3CH3和CH3CH2CH2CH3的结构相似,且分子组成相差2个CH2基团,互为同系物;(4)金刚石和石墨均为碳元素组成的不同单质,互为同素异形体;(5)氕、氘、氚的核电荷数相同,中子数不等,互为同位素;(6)CH3CH2CH2CH(CH3)CH2CH3和CH3CH2CH(CH3)CH(CH3)CH3的分子式相同,但结构不同,互为同分异构体;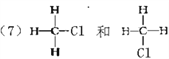 ,分子式相同,结构相同,为同一种物质;则属于同位素的是 (2 )(5),属于同分异构体的是(6),属于同一物质的是(7)。
,分子式相同,结构相同,为同一种物质;则属于同位素的是 (2 )(5),属于同分异构体的是(6),属于同一物质的是(7)。


科目:高中化学 来源: 题型:
【题目】下列有关说法中错误的是( )
A. 第三周期从左往右,简单阳离子的半径依次减小
B. 主族元素中原子半径最小和最大的元素在同一族
C. 王水是浓硝酸和浓盐酸以体积比1∶3混合的溶液
D. 将NH3通入水中制成1L 1mol·L-1的氨水,其中NH3、NH4+的物质的量之和为1mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某无色溶液由Na+、Ag+、Ba2+、Al3+、 [Al(OH)4]-、CO32-、SO32-、SO42-、MnO4-中的若干种组成,取该溶液进行如下实验:
(已知:Al3++3HCO3- =Al(OH)3↓ + 3CO2↑)
①取适量试液,加入过量盐酸,有无色无味气体生成,并得到溶液。
②在①所得溶液中再加入过量碳酸氢铵溶液,有气体生成,同时析出白色沉淀甲。
③在②所得溶液中加入过量氢氧化钡溶液,也有气体生成,并有白色沉淀乙析出。
根据上述现象,回答下列问题:
(1)溶液中一定存在的离子是_____________________________________________;
(2)溶液中一定不存在的离子是______________________________________________;
(3)证明白色沉淀甲是两性氢氧化物的有关离子方程式是________________________;
______________________________________________________________。
(4)判断沉淀乙组成的实验方法是_________________________________________________________________________________________________________________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的分类合理的是( )
碱 | 酸 | 盐 | 酸性氧化物 | |
A | 纯碱 | 盐酸 | 烧碱 | 二氧化硫 |
B | 烧碱 | 硫酸 | 食盐 | 一氧化碳 |
C | 苛性钠 | 醋酸 | 石灰石 | 水 |
D | KOH | 碳酸 | 纯碱 | 三氧化硫 |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将4 mol A气体和2 mol B气体在2 L固定体积的容器中混合,并在一定条件下发生如下反应∶2A(g)+B(g)![]() 2C(g)。若经2s后测得C的浓度为0.6 mol L-1,现有下列几种说法,其中正确的是
2C(g)。若经2s后测得C的浓度为0.6 mol L-1,现有下列几种说法,其中正确的是
A.用物质A表示的反应的平均速率为0.6 mol (L s)-1
B.2 s时物质B的浓度为1.4 mol L-1
C.2 s时物质A的转化率为70%
D.2 s时物质A的体积分数为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原电池是化学对人类的一项重大贡献。
(1)某兴趣小组为研究原电池原理,设计如图A装置。
|
|
A | B |
①a和b不连接时,烧杯中发生反应的离子方程式是 _________________________。
②a和b用导线连接,Cu极为原电池________极(填“正”或“负”),该电极反应式是____________________。
③无论a和b是否连接,Zn片均被腐蚀,若转移了0.2 mol电子, 则理论上Zn片质量减轻________g。
(2)如图是甲烷燃料电池原理示意图B,回答下列问题:
①电池的负极是________(填“a”或“b”)电极,该极的电极反应式为: _________________________。
②电池工作一段时间后电解质溶液的pH__________(填“增大”“减小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了除去粗盐中的Ca2+ 、Mg2+ 、SO42-及泥沙,可将粗盐溶于水,然后进行下列五项操作。其正确的顺序是①过滤 ②加过量的NaOH溶液 ③加适量盐酸 ④加过量Na2CO3溶液 ⑤ 加过量BaCl2 溶液
A.①④②⑤③ B.④①②⑤③ C.②⑤④①③ D.②④①③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】离子液体在有机合成、无机合成等方面有着重要应用。咪唑是合成“离子液体”的一种原料,其结构如图所示。下列有关咪唑说法不正确的是
![]()
A. 化学式C3H4N2
B. 分子中含有一种非极性键和两种极性键
C. 可以发生取代、加成、氧化反应
D. 一氯取代物的同分异构体共有4种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组探究少量Cl2和FeBr2反应的过程。
(1)配制FeBr2溶液:
ⅰ.配制50mL1.0mol/LFeBr2溶液;
ⅱ.上述溶液呈淡黄色。取少量此溶液,向其中滴入KSCN溶液,变为浅红色。
①配制50mL1.0mol/LFeBr2溶液需要的玻璃容器是________________。
②由ⅱ可知,此FeBr2溶液呈黄色的原因是其中含有________,用离子方程式解释产生其原因:_______。
(2)氯气和FeBr2反应实验操作及现象如下:
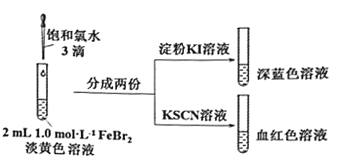
据此甲同学得出结论:少量Cl2既能和Fe2+又能和Br-发生氧化还原反应。
①Cl2和Fe2+发生反应的离子方程式是________________。
②乙同学认为上述实验不能证明Cl2和Br-发生反应,理由是_____________。
③乙同学改进实验如下:在上述FeBr2溶液中加入过量铁粉,取上清液2 mL,向其中滴加3滴饱和氯水后,再加入CCl4,振荡后静置,观察现象。乙得出结论:少量Cl2只与Fe2+反应,不与Br-反应。乙得出该结论依据的实验现象是____________________。
(3)丙同学继续设计实验,探究反应过程:
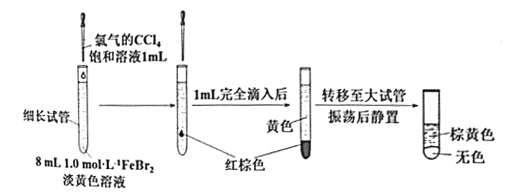
①转移到大试管前CCl4液体中呈红棕色的物质是___________。
②丙通过此实验可得出结论:________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com