
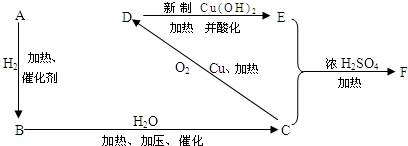
分析 烃A在标准状况下的密度为1.16g/L,其摩尔质量为1.16g/L×22.4L/mol=26g/mol,故A为CH≡CH,乙炔与氢气发生加成反应生成B,B与水反应生成C,C可以连续发生氧化反应,故C为醇,则B为CH2=CH2,乙烯与水发生加成反应生成C为CH3CH2OH,乙醇发生催化氧化生成D为CH3CHO,乙醛进一步氧化生成E为CH3COOH,乙酸与乙醇发生酯化反应生成F为CH3COOCH2CH3,据此解答.
解答 解:烃A在标准状况下的密度为1.16g/L,其摩尔质量为1.16g/L×22.4L/mol=26g/mol,故A为CH≡CH,乙炔与氢气发生加成反应生成B,B与水反应生成C,C可以连续发生氧化反应,故C为醇,则B为CH2=CH2,乙烯与水发生加成反应生成C为CH3CH2OH,乙醇发生催化氧化生成D为CH3CHO,乙醛进一步氧化生成E为CH3COOH,乙酸与乙醇发生酯化反应生成F为CH3COOCH2CH3,
(1)由上述分析可知,A为乙炔,B为乙烯,D为乙醛,故答案为:乙炔;乙烯;乙醛;
(2)由上述分析可知,E的结构简式为CH3COOH,F的结构简式为CH3COOCH2CH3,故答案为:CH3COOH;CH3COOCH2CH3;
(3)B→C是乙烯与水发生加成反应生成乙醇,反应方程式为:CH2=CH2+H2O$\stackrel{催化剂}{→}$CH3CH2OH,故答案为:CH2=CH2+H2O$\stackrel{催化剂}{→}$CH3CH2OH;
(4)C→D是乙醇发生氧化反应生成乙醛,反应方程式为:2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O,
C+E→F是乙酸与乙醇发生酯化反应生成乙酸乙酯,
故答案为:氧化;2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O;酯化.
点评 本题考查有机物的推断,涉及炔、烯烃、醇、醛、羧酸、酯的性质与转化,难度不大,推断A为乙炔,再结合转化中C可以连续发生氧化反应推断,注意对基础知识的理解掌握.


 特高级教师点拨系列答案
特高级教师点拨系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
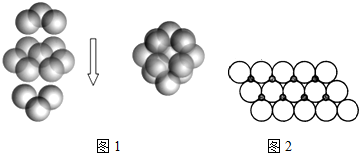
| A. | 晶体在受热熔化过程中一定存在化学键的断裂 | |
| B. | 原子晶体的原子间只存在共价键,而分子晶体内只存在范德华力 | |
| C. | 区分晶体和非晶体最科学的方法是对固体进行X-射线衍射实验 | |
| D. | 非金属元素的原子间只形成共价键,金属元素的原子非金属元素的原子间只形成离子键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蒸馏常用于分离提纯液态有机混合物,温度计的水银球应位于支管口附近 | |
| B. | 核磁共振氢谱通常用于分析有机物的相对分子质量 | |
| C. | 燃烧法通常是研究和确定有机物成分的有效方法之一 | |
| D. | 对有机物分子红外光谱图的研究有助于确定有机物分子中的官能团 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.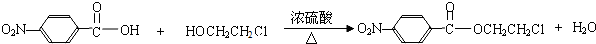 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
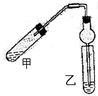 如图(铁架台、铁夹等省略)在试管甲中先加入碎瓷片,再加入2mL 95%的乙醇,并在摇动下缓缓加入2mL浓硫酸,充分摇匀,冷却后再加入2g无水乙酸,用玻璃棒充分搅拌后将试管固定在铁架台上.在试管乙中加入5mL饱和碳酸钠溶液.按如图连接装置,用酒精灯对试管甲加热,当观察到试管乙中有明显现象时停止实验
如图(铁架台、铁夹等省略)在试管甲中先加入碎瓷片,再加入2mL 95%的乙醇,并在摇动下缓缓加入2mL浓硫酸,充分摇匀,冷却后再加入2g无水乙酸,用玻璃棒充分搅拌后将试管固定在铁架台上.在试管乙中加入5mL饱和碳酸钠溶液.按如图连接装置,用酒精灯对试管甲加热,当观察到试管乙中有明显现象时停止实验查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电子数 | B. | 最外层电子数 | C. | 中子数 | D. | 次外层电子数 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
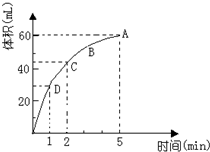 为了研究MnO2与双氧水(H2O2)的反应速率,某学生加入少许的MnO2粉末于 50mL密度为 1.1g/cm3的双氧水溶液中,通过实验测定:在标准状况下放
为了研究MnO2与双氧水(H2O2)的反应速率,某学生加入少许的MnO2粉末于 50mL密度为 1.1g/cm3的双氧水溶液中,通过实验测定:在标准状况下放查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 乙醇能够使蛋白质变性,75%(体积分数)的乙醇溶液可用于医疗消毒 | |
| B. | 乙二醇的水溶液凝固点很低,可用作汽车发动机的抗冻剂 | |
| C. | 光照时乙烷与氯气能发生取代反应,工业上常用该反应生产氯乙烷 | |
| D. | 乙酸( CH3COOH)与硬脂酸(C17H35COOH)互为同系物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com