
| A. | 乙烯的结构式:CHCH | |
| B. | 氯离子的结构示意图: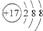 | |
| C. | NH4Cl的电子式: | |
| D. | 碳酸氢钠的电离方程式:NaHCO3═Na++H++CO32- |
分析 A.乙烯结构简式中碳碳双键不能省略
B.氯离子的核电荷数为17,最外层得到8电子稳定结构;
C.氯离子为阴离子,其电子式中需要标出所带电荷及最外层电子;
D.碳酸氢钠为弱电解质,在溶液中完全电离出钠离子和碳酸氢根离子,碳酸氢根离子不能拆开.
解答 解:A.乙烯结构简式中碳碳双键不能省略,乙烯的结构简式为CH2═CH2,故A错误;
B.氯离子的核电荷数为17,最外层达到8电子稳定结构,其离子结构示意图为 ,故B正确;
,故B正确;
C.氯化铵为离子化合物,铵根离子和氯离子都需要标出最外层电子及所带电荷,其正确的电子式为 ,故C错误;
,故C错误;
D.碳酸氢钠完全电离,碳酸氢根离子不能拆开,其正确的电离方程式为NaHCO3═Na++HCO3-,故D错误;
故选B.
点评 本题考查了常见化学用语的判断,题目难度中等,明确常见化学用语的概念及书写原则为解答关键,试题侧重考查学生的分析能力及规范答题能力.


科目:高中化学 来源: 题型:解答题
 已知A、B、C、D、E五种元素的原子序数依次递增,A、B、C、D位于短周期.A位于周期表的s区,其原子中电子层数和未成对电子数相同;B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同;D原子最外层电子数是次外层电子数的3倍.E有“生物金属”之称,E4+和氩原子的核外电子排布相同.
已知A、B、C、D、E五种元素的原子序数依次递增,A、B、C、D位于短周期.A位于周期表的s区,其原子中电子层数和未成对电子数相同;B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同;D原子最外层电子数是次外层电子数的3倍.E有“生物金属”之称,E4+和氩原子的核外电子排布相同.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素编号 | 元素特征信息 |
| A | 其单质是密度最小的物质 |
| B | 阴离子带两个单位负电荷,单质是空气的主要成分之一 |
| C | 其阳离子与B的阴离子有相同的电子层结构,电离能(I)数据依次为:I1=490kJ/mol-1,I2=4562kJ/mol-1,I3=6912kJ/mol-1… |
| D | 其氢氧化物和氧化物都有两性,与C同周期 |
| E | 在第四周期元素原子中,其所含不成对电子数最多 |
 ;E基态原子的电子排布式1s22s22p63s23p63d54s1.
;E基态原子的电子排布式1s22s22p63s23p63d54s1. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
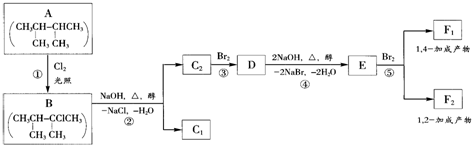
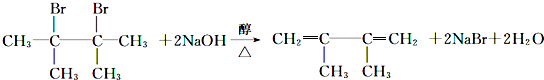 .
.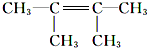 .F1的结构简式是
.F1的结构简式是 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用铁片和稀硫酸反应制取氢气时,改用98%的浓硫酸可以加快产生氢气的速率 | |
| B. | 100 mL 2 mol•L-1的盐酸跟锌片反应,加入适量的氯化钠溶液,反应速率不变 | |
| C. | SO2的催化氧化是一个放热反应,升高反应的温度,反应速率减慢 | |
| D. | 用锌和稀硫酸反应制取H2时,滴加几滴硫酸铜溶液能加快反应速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ① | B. | ② | C. | ③ | D. | 无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 材料是人类赖以生存和发展的重要物质基础.
材料是人类赖以生存和发展的重要物质基础.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com