
科目:高中化学 来源: 题型:阅读理解
| 物质 | (CH3CO)2O | C6H5CHO | C6H5CH=CHCOOH | CH3COOH |
| 沸点 | 139℃ | 179℃ | 300℃ | 117.9℃ |



查看答案和解析>>
科目:高中化学 来源: 题型:
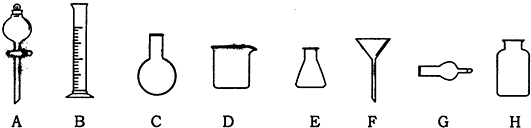
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关实验的叙述中正确的是( )

A.用pH试纸粗略测定饱和氯水的pH
B.做完某种物质的焰色反应实验后,用稀盐酸洗净铂丝,并在火焰上灼烧至没有颜色后,再进行其他物质的焰色反应实验
C.实验室常用如图所示的装置制取少量乙酸乙酯
D.在含FeCl2杂质的FeCl3溶液中通入足量Cl2后,加热蒸干即得纯净的FeCl3固体
查看答案和解析>>
科目:高中化学 来源:2014届江苏省海门市高三第一次诊断考试化学试卷(解析版) 题型:实验题
下列有关物质性质应用的说法正确的是
A.SO2具有漂白性,可用作熏蒸粉丝使其增白
B.常温下二氧化硅不与强酸反应,可用石英容器盛放氢氟酸
C.铜的金属活泼性比铁的弱,可在铁船闸上装若干铜块以减缓其腐蚀
D.氧化铝熔点很高,可用作制造高温耐火材料,如制耐火砖、坩埚等常用作催熟剂、除草剂等,实验室用卤块(主要成分为MgCl2·6H2O,含有MgSO4、FeCl2等杂质)制备少量Mg(ClO3)2·6H2O的流程如下:

已知:几种化合物的溶解度(S)随温度(T)变化曲线如下图所示。

(1)过滤时主要玻璃仪器有 。加入BaCl2的目的是除去杂质离子,检验已沉淀完全的方法是: 。
(3)“调节pH=4”可选用的试剂是 (填编号)
①MgO ②CuO ③稀NaOH溶液
④Mg ⑤稀硫酸 ⑥MgCO3
(4)反应II为:MgCl2+2NaClO3=Mg(ClO3)2+2NaCl↓,再进一步制取Mg(ClO3)2·6H2O的实验步骤依次为:① ;②趁热过滤;③ ;④过滤、洗涤、干燥。
(5)产品中Mg(ClO3)2·6H2O含量的测定:
步骤1:准确称量m g产品配成100 mL溶液。
步骤2:取10 mL溶液于锥形瓶中,加入10 mL稀硫酸和20 mL 1.000 mol·L-1的FeSO4溶液,微热。
步骤3:冷却至室温,用0.100 mol·L-1 K2Cr2O7标准溶液滴定未被氧化的Fe2+。记录消耗K2Cr2O7溶液的体积。
①步骤2中发生反应的离子方程式为: 。
②若配制K2Cr2O7标准溶液时未洗涤烧杯,则产品中Mg(ClO3)2·6H2O的含量会 。(填“偏高”、“偏低” 或“不变”)。
查看答案和解析>>
科目:高中化学 来源:09-10年新余一中高二下学期第二次段考化学卷 题型:选择题
下列有关实验的叙述中正确的是
A.用pH试纸粗略测定饱和氯水的pH
B.做完某种物质的焰色反应实验后,用稀盐酸洗净铂丝,并在火焰上灼烧至没有颜色后,再进行其他物质的焰色反应实验

C.实验室常用如图所示的装置制取少量乙酸乙酯
D.在含FeCl2杂质的FeCl3溶液中通入足量Cl2后,加热蒸干即得纯净的FeCl3固体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com