
【题目】在产生了AgCl沉淀的试管中,加入KI溶液,白色沉淀变为黄色。下列说法正确的是( )
A.该实验说明I-还原性比Cl-强B.该实验说明Ksp(AgCl)<Ksp(AgI)
C.该实验说明AgI溶解度比AgCl小D.KI的加入对AgCl的溶解平衡没有影响
【答案】C
【解析】
A. AgCl沉淀变为AgI沉淀,该反应没有元素化合价变化,不是氧化还原反应,不能比较离子的还原性强弱,故不选A;
B.产生了AgCl沉淀的试管中,加入KI溶液,白色沉淀变为黄色,AgCl沉淀变为AgI沉淀,说明Ksp(AgCl)>Ksp(AgI),故不选B;
C.AgCl(s)![]() Ag+(aq)+Cl-(aq),加入KI,I-结合Ag+生成AgI沉淀,使c(Ag+)减小,AgCl的溶解平衡向右移动, AgCl转化为AgI,说明AgI溶解度更小,故C正确;
Ag+(aq)+Cl-(aq),加入KI,I-结合Ag+生成AgI沉淀,使c(Ag+)减小,AgCl的溶解平衡向右移动, AgCl转化为AgI,说明AgI溶解度更小,故C正确;
D. AgCl(s)![]() Ag+(aq)+Cl-(aq),加入KI,I-结合Ag+,使c(Ag+)减小,AgCl的溶解平衡向右移动,故D错误;
Ag+(aq)+Cl-(aq),加入KI,I-结合Ag+,使c(Ag+)减小,AgCl的溶解平衡向右移动,故D错误;
故答案选C。


 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案科目:高中化学 来源: 题型:
【题目】在容积一定的密闭容器中发生可逆反应:A(g)+2B(g)2C(g);ΔH>0(表示吸热)。平衡移动关系如图所示,下列说法正确的是( )
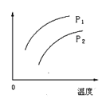
A.P1>P2,纵坐标指C的质量分数B.P1<P2,纵坐标指A的质量分数
C.P1<P2,纵坐标指A的转化率D.P1<P2,纵坐标指混合气体的平均摩尔质量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A.1.0 mol·L-1的KNO3溶液中:H+、Fe2+、Cl-、![]()
B.使紫色石蕊溶液变红的溶液中:![]() 、Ba2+、
、Ba2+、![]() 、Cl-
、Cl-
C.pH=12的溶液中:K+、Na+、CH3COO-、Br-
D.滴加几滴KSCN溶液显血红色的溶液中:![]() 、Mg2+、I-、Cl-
、Mg2+、I-、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物X和Y可作为“分子伞”给药载体的伞面和中心支撑架(未表示出原子或原子团的空间排列)。
X(C24H40O5):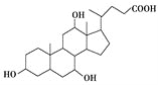
Y:H2NCH2CH2CH2NHCH2CH2CH2CH2NH2
下列叙述错误的是( )
A.1 mol X在浓硫酸作用下发生消去反应,最多生成3 mol H2O
B.1 mol Y发生类似酯化的反应,最多消耗2 mol X
C.X与足量HBr反应,所得有机物的分子式为C24H37O2Br3
D.Y与癸烷的分子链均呈锯齿形,但Y的极性较强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环丙烷可作为全身麻醉剂,环己烷是重要的有机溶剂。下表是部分环烷烃及烷烃衍生物的结构简式、键线式和某些有机化合物的反应式(其中Pt、Ni是催化剂)。
结构简式 |
|
|
|
键线式 |
|
|
|
①![]() +H2
+H2![]()
![]()
②![]() +H2
+H2![]()
![]()
③![]() +H2
+H2![]()
![]()
④![]() +KMnO4
+KMnO4![]()
![]() +
+![]() +Mn2+
+Mn2+
回答下列问题:
(1)环烷烃与___________是同分异构体。
(2)从反应①~③可以看出,最容易发生开环加成反应的环烷烃是______(填名称),判断依据为_________。
(3)环烷烃还可与卤素单质、卤化氢发生类似的开环加成反应,如环丁烷与HBr在一定条件反应,其化学方程式为(不需注明反应条件)____________。
(4)写出鉴别环丙烷与丙烯的一种方法:试剂___________;现象与结论 __________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值。下列说法正确的是( )
A. 0.1molCH4和0.1molCl2充分反应,生成的C-Cl键和H-Cl键的数目均为0.2NA
B. 7.8gNa2S和Na2O2的混合物中所含阴离子的数目等于0.2NA
C. 18g固态水(冰)中含有的氢键的数目为2NA
D. 25℃时,Ksp(AgI)=1.0×10-16,则AgI饱和溶液中Ag+数目为1.0×10-8NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,Fe(OH)2和Cu(OH)2的饱和溶液中,金属阳离子的物质的量浓度的负对数[一lg c(M2+)]与溶液pH的变化关系如图所示,已知该温度下,Ksp[Cu(OH)2]2],下列说法正确的是 ( )

A. b线表示Fe(OH)2饱和溶液中的变化关系,且Ksp[Fe(OH)2]=10-15.1
B. 当Fe(OH)2和Cu(OH)2沉淀共存时,溶液中:C(Fe2+):C(Cu2+):1:104.6
C. 向X点对应的饱和溶液中加入少量NaOH,可转化为Y点对应的溶液
D. 除去CuSO4溶液中含有的少量Fe2+,可加入适量Cu0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应N2O4(g)![]() 2NO2(g) ΔH=+57kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化的曲线如图所示。下列说法正确的是
2NO2(g) ΔH=+57kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化的曲线如图所示。下列说法正确的是
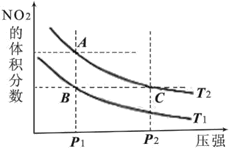
A.A、C两点的反应速率:A>C
B.A、C两点气体的颜色:A深,C浅
C.A、B两点气体的平均相对分子质量:A>B
D.B、C两点化学平衡常数:B<C
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com