
【题目】某新型电池,以NaBH4(B的化合价为+3价)和H2O2作原料,该电池可用作深水勘探等无空气环境电源,其工作原理如下图所示。下列说法不正确的是

A. 每消耗3mol H2O2,转移6mol e-
B. 电池工作时Na+从b极区移向a极区
C. b极上的电极反应式为:H2O2 + 2e-= 2OH-
D. a极上的电极反应式为:BH4-+ 8OH--8e-=BO2-+6H2O
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】在一密闭容器中进行反应:C(s) + H2O(g)= CO(g) + H2(g),下列条件的改变对反应速率几乎无影响的是( )
A.增加CO的量B.保持体积不变,充入N2,使体系的压强增大
C.将容器的体积缩小一半D.保持压强不变,充入N2,使容器的体积变大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:①向KMnO4晶体滴加浓盐酸,产生黄绿色气体;②向FeCl2溶液中通入少量实验①产生的气体,溶液变黄色;③取实验②生成的溶液滴在淀粉KI试纸上,试纸变蓝色。下列判断不正确的是
A.上述实验证明氧化性:MnO4->Cl2>Fe3+>I2
B.实验①中,用160 mL 10 mol/L的高锰酸钾溶液与足量KMnO4充分反应,标准状况下可制得11.2 L的Cl2
C.实验①生成的气体能使湿润的淀粉KI试纸变蓝
D.实验①中要收集纯净干燥的黄绿色气体,应将气体依次通过饱和食盐水和浓硫酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列说法不正确的是
A. 常温常压下,35.5g的氯气与足量的氢氧化钙溶液完全反应,转移的电子数为0.5NA
B. 60g甲酸甲酯和葡萄糖的混合物含有的碳原子数目为2NA
C. 标准状况下,2.24L PH3与3.4gH2S气体分子所含电子数目均为1.8NA
D. 已知合成氨反应N2(g)+3H2(g)![]() 2NH3(g) △H= -92.4kJ/mol当该反应生成NA个NH3分子时,反应放出的热量小于46.2kJ
2NH3(g) △H= -92.4kJ/mol当该反应生成NA个NH3分子时,反应放出的热量小于46.2kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素周期表的形式多种多样,如图是扇形元素周期表的一部分,对比中学常见元素周期表,分析其元素的填充规律,判断下列说法正确的是

A.③元素形成的单质晶体均属于原子晶体
B.②、⑦、⑧对应的简单离子半径依次减小
C.②⑤形成的化合物阴阳离子个数比可能为1∶1
D.④元素的气态氢化物易液化,是因为其分子间存在氢键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验操作的叙述错误的是
A.过滤操作中,漏斗的尖端应接触烧杯内壁
B.向容量瓶中转移液体时,引流用的玻璃棒可以接触容量瓶内壁
C.配制5%NaCl溶液时,必须用到的玻璃仪器是容量瓶、烧杯、胶头滴管、玻璃棒
D.分液漏斗、容量瓶及滴定管使用前都必须检漏
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有常见的A-J物质存在如下转化关系示意图(反应条件己略去),
已知通常情况下A、H 为固态金属单质,B、D为气态非金属单质,E为淡黄色固体,F为无色液体,J为红褐色沉淀.请回答下列问题:
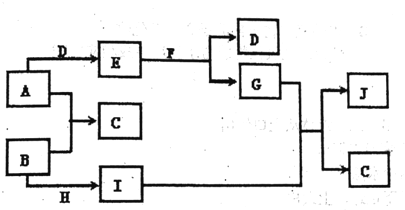
(1)写出下列物质的化学式:A_____;C____; J ______;
(2)转化I+G![]() J+C的反应类型为______。
J+C的反应类型为______。
(3)E中阴阳离子个数比与_______相同(填字母)
a.MgCl2 b.Na2O c.NaCl d.K2SO4
(4)写出下列反应的化学方程式:
① E+F![]() ________;
________;
② B+G![]() _________。
_________。
(5)写出E的一种用途:_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组探究在加热条件下FeSO4分解的气体产物及相关性质。已知:SO2的沸点为-10℃、SO3的沸点为44.8℃。
Ⅰ.用如图所示装置设计实验,验证分解FeSO4生成的气态产物。

(1)实验前必须进行的操作是_______________________。
(2)按气流方向连接各仪器,用字母表示接口的连接顺序:a→_________________。
(3)若观察到装置丙中有无色液体产生,装置丁中溶液变成无色,则 FeSO4分解的化学方程式为____________________。
Ⅱ.为探究SO2使品红溶液褪色的原理,进行如下实验:
实验1:将稀盐酸和NaOH溶液分别滴入品红水溶液中。观察到前者溶液颜色变浅,但未能完全褪色,后者溶液颜色几乎不变。
实验2:在滴有稀盐酸和NaOH溶液的两份品红水溶液中分别通入SO2。观察到前者溶液逐渐褪色,后者溶液很快褪色。
实验3:在两份品红水溶液中分别加入一小粒Na2SO3固体和NaHSO3固体,前者溶液很快褪色,后者溶液褪色很慢。
(1)由实验1可推测品红水溶液呈________性。
(2)由实验2、3可推知,使品红水溶液褪色的主要微粒是_________(填化学式)。
(3)若将SO2通入品红的无水乙醇溶液,试预测可能出现的现象________________。
(4)加热溶有Na2SO3的品红水溶液,发现不能恢复红色,试解释原因____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列固体混合物与过量的稀H2SO4反应,能产生气泡并有沉淀生产的是 ( )
A. NaHCO3和Al(OH)3 B. BaCl2和NaCl
C. HClO3和K2SO4 D. Na2SO3和BaCO3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com