
将磁性氧化铁放入稀HNO3中可发生如下反应:3Fe3O4+28HNO3═9Fe(NO3)x+NO↑+14H2O下列判断合理的是( )
|
| A. | Fe(NO3)x中的x为2 |
|
| B. | 反应中每还原0.4mol氧化剂,就有1.2mol电子转移 |
|
| C. | 稀HNO3在反应中只表现氧化性 |
|
| D. | 磁性氧化铁中的所有铁元素全部被氧化 |
考点:
氧化还原反应;氧化还原反应的电子转移数目计算.
专题:
氧化还原反应专题.
分析:
反应3Fe3O4+28HNO3═9Fe(NO3)x+NO↑+14H2O中,Fe元素的化合价升高,N元素的化合价降低,以此来解答.
解答:
解:A.由N原子守恒可知,28=9x+1,解得x=3,故A错误;
B.N元素的化合价由+5价降低为+2价,则反应中每还原0.4mol氧化剂,就有0.4mol×(5﹣2)=1.2mol电子转移,故B正确;
C.稀HNO3在反应中生成硝酸盐和NO,则表现酸性和氧化性,故C错误;
D.磁性氧化铁中的Fe有+2价和+3价,则部分被氧化,故D错误;
故选B.
点评:
本题考查氧化还原反应,明确元素的化合价变化及氧化还原反应中转移的电子数的关系、原子守恒等时解答本题的关键,难度不大.


科目:高中化学 来源: 题型:
X、Y、Z、W均为短周期元素,它们在元素周期表中相对位置如图所示,若Z原子的最外层电子数是第一层电子数的3倍,下列说法正确的是( )
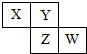
A. Z单质与氢气反应较Y剧烈
B. 最高价氧化物对应水化物酸性W比Z强
C. X单质氧化性强于Y单质
D. X与W的原子核外电子数相差9
查看答案和解析>>
科目:高中化学 来源: 题型:
一般情况下胶体稳定,胶体微粒不易聚集,主要原因是( )
A.胶体有丁达尔现象
B.胶体有布朗运动
C.胶体微粒因吸附带电荷离子而带电,带同种电荷的微粒间相互排斥
D.胶体微粒直径在1~100nm之间,微粒小,不受重力作用
查看答案和解析>>
科目:高中化学 来源: 题型:
类比(比较)是研究物质性质的常用方法之一,可预测许多物质的性质.但类比是相对的,不能违背客观实际.下列各说法中正确的是( )
|
| A. | 根据化合价Fe3O4可表示为FeO•Fe2O3,则Pb3O4也可表示为PbO•Pb2O3 |
|
| B. | CaC2能水解:CaC2+2H2O=Ca(OH)2+C2H2↑,则Al4C3也能水解:Al4C3+12H2O=4Al(OH)3+3CH4↑ |
|
| C. | Cl2与Fe加热生成FeCl3,则I2与Fe加热生成FeI3 |
|
| D. | SO2通入BaCl2溶液不产生沉淀,则SO2通入Ba(NO3)2溶液也不产生沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
用NA表示阿伏加德罗常数的值,则下列叙述正确的是( )
|
| A. | 常温下,4.48L N2和O2的混合气体中所含原子数为0.4NA |
|
| B. | 常温下,1.0L1.0mol•L﹣1 NaAlO2溶液中含有的氧原子数为2NA |
|
| C. | 7.8g Na2S和Na2O2的混合物中含有的阴离子数等于0.1NA |
|
| D. | 0.1mol Fe参加氧化还原反应,转移的电子数目一定是0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知反应:
①SO3+H2O=H2SO4
②Cl2+H2O=HCl+HClO
③2F2+2H2O=4HF+O2↑
④2Na+2H2O=2NaOH+H2↑
⑤2Na2O2+2H2O=4NaOH+O2↑
⑥SiO2+2NaOH=Na2SiO3+H2O
(1)上述反应中不属于氧化还原反应的有 (填序号,下同).H2O被氧化的是 H2O被还原的是 .属于氧化还原反应,但其中的H2O既不被氧化,又不被还原的是 .
(2)写出方程式②的离子方程式 .
(3)标出方程式④的电子转移的方向和数目 .
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)下列各组物质 ①O2和O3 ②12C和14C ③CH3CH2CH2CH3和(CH3)2CHCH3
④干冰和SiC ⑤金刚石和SiO2
它们的晶体属于分子晶体的是 ,互为同位素的是 ,属于原子晶体的是 .
(2)配离子[TiCl(H2O)5]2+的中心离子的符号为 ,配位数为 .
(3)写出下列方程式
①甲酸(HCOOH)与甲醇(CH3OH)在浓硫酸加热条件下发生酯化反应的化学方程式
②苯与液溴在溴化铁催化剂下反应方程式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)原子序数11~17的元素,自钠到氯,电子层数相同,最外层电子数从 增加到 ,随着核电荷数依次递增,原子半径依次 ,核对外层电子的引力逐渐 ,失电子能力逐渐 ,得电子能力逐渐 ,因此,金属性逐渐 ,非金属性逐渐 .
(2)元素金属性的强弱,可以从它的单质与水或酸的反应置换氢的 程度,以及它的最高价氧化物的水化物的 强弱来判断.元素非金属性的强弱,可以从它的最高价氧化物的水化物的 强弱,或它的单质跟氢气生成气态氢化物的 及氢化物的 来判断.
(3)元素的性质随着原子序数的递增而呈 的变化,这个规律叫做元素周期律.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com