
 ;⑤的反应类型为取代反应.
;⑤的反应类型为取代反应.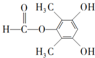 、
、 .
. 为原料制备
为原料制备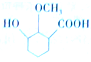 的合成路线
的合成路线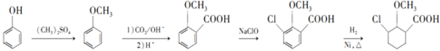
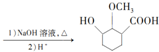
 (无机试剂可任选)
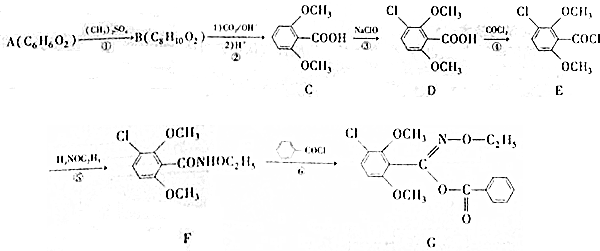
(无机试剂可任选) 分析 (1)(2)比较B的分子式和C的结构简式可知,B为 ,根据A的分子式及A转化成B的条件可知,A为
,根据A的分子式及A转化成B的条件可知,A为 ,A发生取代反应生成 B,比较E和F的结构简式可知⑤的反应类型;
,A发生取代反应生成 B,比较E和F的结构简式可知⑤的反应类型;
(3)根据条件Ⅰ.能发生银镜反应也能与FeCl3溶液发生显色反应,说明有醛基和酚羟基,Ⅱ.核磁共振氢谱有4组峰且峰面积之比为6:2:1:1,结合C的结构简式可知C的同分异构体的种类;其中能发生水解反应的,说明有酯基,据此书写其结构简式;
(4)依据西斗星的合成路线,以 为原料制备
为原料制备 可以将
可以将 与硫酸甲酯反应生成甲苯醚,再发生类似西斗星的合成路线中的②和③反应,再与氢气加成后碱性水解、酸化可得
与硫酸甲酯反应生成甲苯醚,再发生类似西斗星的合成路线中的②和③反应,再与氢气加成后碱性水解、酸化可得 ,据此答题;
,据此答题;
解答 解:(1)根据A的分子式及A转化成B的条件可知,A为 ,A的名称为间苯二酚或1,3-苯二酚,根据C的结构简式可知,C中含氧官能团为羧基和醚键,
,A的名称为间苯二酚或1,3-苯二酚,根据C的结构简式可知,C中含氧官能团为羧基和醚键,
故答案为:间苯二酚或1,3-苯二酚;羧基和醚键;
(2)比较B的分子式和C的结构简式可知,B为 ,比较E和F的结构简式可知⑤的反应类型为取代反应,
,比较E和F的结构简式可知⑤的反应类型为取代反应,
故答案为: ;取代反应;
;取代反应;
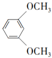
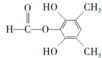
(3)根据条件Ⅰ.能发生银镜反应也能与FeCl3溶液发生显色反应,说明有醛基和酚羟基,Ⅱ.核磁共振氢谱有4组峰且峰面积之比为6:2:1:1,结合C的结构简式可知符合条件的同分异构体为 、
、 、
、 、
、 、
、 、
、 ,共6种,其中能发生水解反应的,说明有酯基,其结构简式为
,共6种,其中能发生水解反应的,说明有酯基,其结构简式为 、
、 ,
,
故答案为:6; 、
、 ;
;
;
(4)依据西斗星的合成路线,以 为原料制备
为原料制备 可以将
可以将 与硫酸甲酯反应生成甲苯醚,再发生类似西斗星的合成路线中的②和③反应,再与氢气加成后碱性水解、酸化可得
与硫酸甲酯反应生成甲苯醚,再发生类似西斗星的合成路线中的②和③反应,再与氢气加成后碱性水解、酸化可得 ,其合成路线为
,其合成路线为
 ,
,
故答案为:
 .
.
点评 本题考查有机物的推断与合成,成分利用转化关系中有机物的进行进行分析解答,较好的考查学生的分析推理能力、获取信息能力、知识迁移运用能力,难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
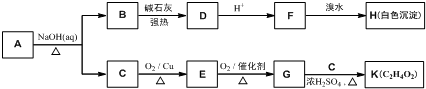

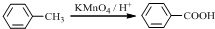
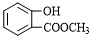 .
.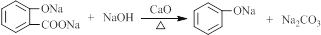 .
.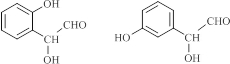 (写结构简式).
(写结构简式).查看答案和解析>>
科目:高中化学 来源: 题型:解答题
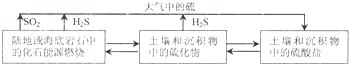
| 25℃ | 饱和H2S溶液 | FeS | SnS | |
| pH | 3.9 | 3.0(开始沉淀 | 5.5(沉淀完全) | 1.6(沉淀完全) |
| Ksp | 6.3×10-18 | 1.0×10-25 | ||
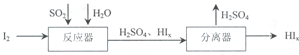
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4L空气中O2、N2分子数为NA | |
| B. | 0.1mol羟基中所含电子数目为NA | |
| C. | 钠与氧气反应时,每消耗4.6g钠时生成的阴离子数目为0.1NA | |
| D. | 25℃时,1.0L pH=13的Ba(OH)2溶液中含有的OH-数为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 反应 | 大气固氮N2(g)+O2(g)?2NO(g) | |
| 温度/℃ | 27 | 2260 |
| K | 3.84×10-31 | 1 |
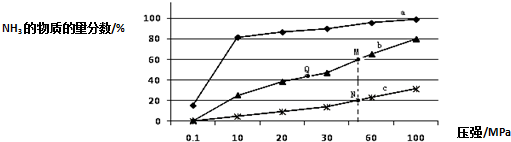
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaHCO3溶液显弱酸性 | |
| B. | 该溶液中K+、Al3+、H+、SO${\;}_{4}^{2-}$可以大量共存 | |
| C. | 加水稀释该溶液,溶液中$\frac{c(HC{O}_{3}^{-})}{c(C{O}_{3}^{2-})}$增大 | |
| D. | 向该溶液中加入足量的氢氧化钙溶液的离子方程式为:2HCO${\;}_{3}^{-}$+Ca2++2OH-═CaCO3↓+CO${\;}_{3}^{2-}$+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
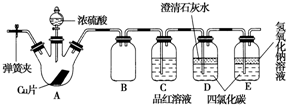
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com