
| A. | 铅蓄电池属于二次电池 | |
| B. | 氢氟酸可用于蚀刻玻璃是因为其具有强酸性 | |
| C. | 为了防止食品受潮,常在食品包装袋中放入活性铁粉 | |
| D. | 用于制光缆的光导纤维是新型有机高分子材料 |
科目:高中化学 来源: 题型:解答题
 向100mL NaOH溶液中逐渐通入一定量的CO2(假设溶液体积不变),测得最后溶液的pH>7.
向100mL NaOH溶液中逐渐通入一定量的CO2(假设溶液体积不变),测得最后溶液的pH>7.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  能作为SO2的干燥装置 | |
| B. | 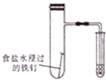 验证铁钉的吸氧腐蚀 | |
| C. | 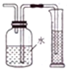 可用于测量Cu与浓硝酸反应生成NO2的体积 | |
| D. | 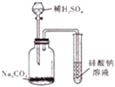 可证明酸性:H2SO4>H2CO3>H2SiO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 煤经过气化和液化等物理变化可转化为清洁燃料 | |
| B. | 为了提高酒精的杀菌消毒效果,医院常用体积分数为100%的酒精 | |
| C. | 用浸泡过酸性高锰酸钾溶液的硅藻土吸收水果释放的乙烯,可达到水果保鲜的目的 | |
| D. | 石墨烯是一种从石墨材料中用“撕裂”方法“剥离”出的单层碳原子面材料,石墨烯和乙烯都属于烯烃 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.00molNaCl固体中含有6.02×1023个NaCl分子 | |
| B. | 46gNO2和N2O4混合气体中含有原子总数为3NA | |
| C. | 1molFe2+与足量的H2O2溶液反应,转移2NA个电子 | |
| D. | 25℃,pH=13的NaOH溶液中含有OH-的数目为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 在上述条件下发生反应,得到的最终产物结构式分别是:
在上述条件下发生反应,得到的最终产物结构式分别是: 、
、
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2、I2、HI的浓度相等 | B. | H2、I2、HI的浓度之比为1:1:2 | ||
| C. | 混合气体的平均相对分子质量不变 | D. | 混合气体的颜色不再改变 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com