
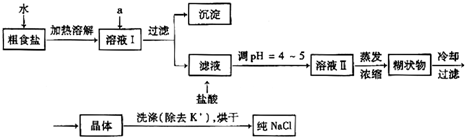
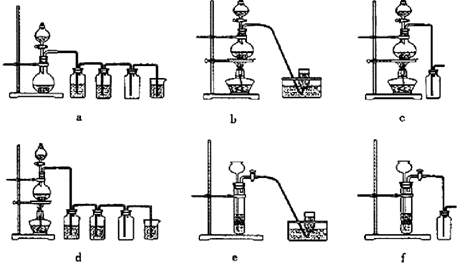
粗食盐常含有少量K+、Ca2+、Mg2+、Fe3+、SO42-等杂质离子,实验室提纯NaCl的流程如下:
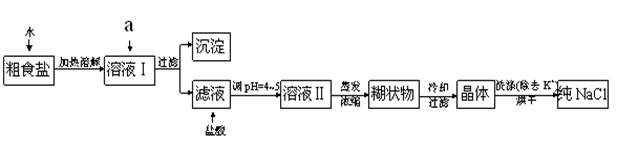
提供的试剂:饱和Na2CO3溶液、 饱和K2CO3溶液 、NaOH溶液、 KOH溶液、 BaCl2溶液 、Ba(NO3)2溶液
(1)欲除去溶液中的Ca2+、Mg2+、Fe3+、SO42-离子,选出a所代表的各种试剂,按滴加顺序依次为 (填化学式);
(2)蒸发浓缩溶液Ⅱ得到的糊状物的化学成分最多的是(填化学式);
(3)用提纯过的NaCl固体来配制480 mL 0.4 mol·L-1NaCl溶液时,所用仪器除烧杯、药匙、玻璃棒、天平、胶头滴管外还有 (填仪器名称);需NaCl g。
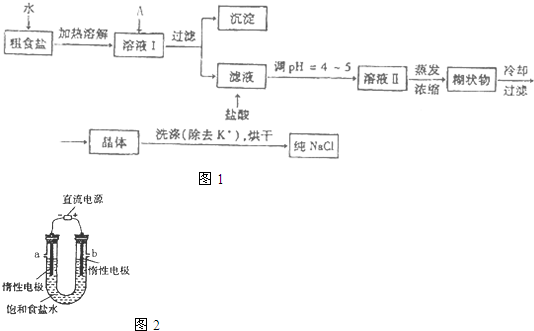
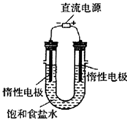
(4)电解饱和食盐水的装置如图所示:

若收集到的H2为2 L,则同样条件下收集到的Cl2体积 (填“>”、“=”或“<”)2 L,其原因是: (文字描述);若将此装置的b口密封住,则电解一段时间后,U型管中可以获得一种消毒液,写出获得此消毒液的一个总反应方程式: 。
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

| ||

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com