
科目:高中化学 来源: 题型:解答题
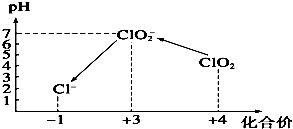 ClO2气体是一种常用的消毒剂,我国从2000年起逐步用ClO2代替氯气对饮用水进行消毒.
ClO2气体是一种常用的消毒剂,我国从2000年起逐步用ClO2代替氯气对饮用水进行消毒.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 草酸的摩尔质量是90g/mol | |
| B. | 1mol草酸中含有6.02×1023个分子 | |
| C. | 45g草酸中含有1.204×1024个氧原子 | |
| D. | 1mol草酸在标准状况下的体积约为22.4L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 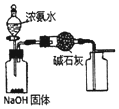 用图装置,制取干燥纯净的NH3 | |
| B. |  用图装置,实验室制备Fe(OH)2 | |
| C. | 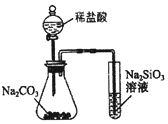 用图所示实验,可比较氯、碳、硅三种元素的非金属性强弱 | |
| D. | 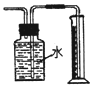 用图装置测量Cu与浓硝酸反应产生气体的体积 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 单质的沸点:W>Y | B. | 简单离子的半径:W>X | ||
| C. | 阴离子的还原性:Z<W | D. | Y与Z能形成离子化合物Y2Z2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 所有含碳元素的物质都是有机化合物 | |
| B. | 有机化合物是指所有含碳的化合物 | |
| C. | CO、CO2是含碳化合物,所以它们是有机化合物 | |
| D. | 有机物中一定含碳元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.2 mol过氧化氢完全分解转移的电子数目为0.4NA | |
| B. | 300 mL 2 mol/L蔗糖溶液中所含分子数为0.6 NA | |
| C. | 在常温常压下,17 g硫化氢所含质子数目为8 NA | |
| D. | 在标准状况下,2.24 L二氧化硫与氧气混合气体中所含氧原子数为0.2 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
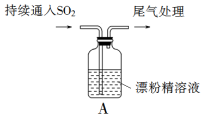 某化学兴趣小组的同学们对SO2通入漂粉精溶液的反应进行实验探究:
某化学兴趣小组的同学们对SO2通入漂粉精溶液的反应进行实验探究:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
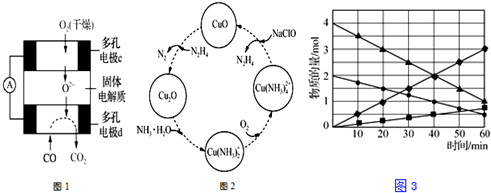
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com