
下列各组物质中,都是强电解质的是( )
|
| A. | HBr、HCl、BaSO4 | B. | NH4Cl、CH3COOH、Na2S |
|
| C. | NaOH、Ca(OH)2、NH3•H2O | D. | HClO、NaF、Ba(OH)2 |
考点:
强电解质和弱电解质的概念.
专题:
物质的分类专题.
分析:
强电解质是指:在水溶液中或熔融状态下,能够完全电离的化合物.即溶于水的部分或者熔融状态时,可以完全变成阴阳离子的化合物.一般是强酸、强碱和大部分盐类.
弱电解质是指:在水溶液里部分电离的电解质,包括弱酸、弱碱、水与少数盐;
解答:
解:A、HBr、HCl、BaSO4是在水中完全电离成离子的化合物,所以属于强电解质,故A正确.
B、CH3COOH在水中只有部分电离,所以属于弱电解质,故B错误.
C、NH3•H2O在水中只有部分电离,所以属于弱电解质,故C错误.
D、HClO在水中只有部分电离,所以属于弱电解质,故D错误.
故选:A;
点评:
本题考查了强电解质的判断,难度不大,熟记常见的强电解质是解题的关键.


 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案科目:高中化学 来源: 题型:
化学用语是学习化学的重要工具,下列用来表示物质变化的化学用语中,正确的是( )
A.向Mg(HCO2)3溶液中滴加过量的NaOH溶液的离子方程式:Mg2++2HCO3﹣+2OH﹣═MgCO3↓+CO32﹣+2H2O
B.向NH4Al(SO4)2溶液中滴入Ba(OH)2溶液恰好使SO42﹣完全沉淀的离子方程式:2Ba2++NH4++Al3++2SO42﹣+4OH﹣═Al(OH)3↓+NH3·H2O+2BaSO4↓
C.用稀醋酸除去铜绿的离子方程式:4H++Cu2(OH)2CO3=2Cu2++CO2↑+3H2O
D.已知:
| 共价键 | C﹣C | C=C | C﹣H | H﹣H |
| 键能/kJ·mol﹣1 | 348 | 610 | 413 | 436 |
则可以计算出反应 的△H为﹣384 kJ·mol﹣1
的△H为﹣384 kJ·mol﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应的离子方程式书写正确的是( )
|
| A. | Cu与浓硝酸的反应:Cu+2H+═Cu2++H2↑ |
|
| B. | FeCl2溶液与Cl2的反应:Fe2++Cl2═Fe3++2Cl﹣ |
|
| C. | H2SO4溶液与KOH溶液的反应:H++OH﹣═H2O |
|
| D. | CuCl2溶液与NaOH溶液的反应:CuCl2+2OH﹣═Cu(OH)2↓+2Cl﹣ |
查看答案和解析>>
科目:高中化学 来源: 题型:
25℃时,有pH=3的醋酸和pH=3的硫酸两种溶液,下列叙述正确的是( )
|
| A. | 两溶液中水电离出的c(H+)=1×10﹣11mol/L |
|
| B. | 加水稀释100倍后两溶液pH仍相同 |
|
| C. | 醋醋中c(CH3COO﹣)与硫酸中的c(SO42﹣)相同 |
|
| D. | 两溶液中分别加入足量锌片放出H2体积相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
|
| A. | 在一定温度下的AgCl水溶液中,Ag+和Cl﹣浓度的乘积是一个常数 |
|
| B. | AgCl的Ksp=1.8×10﹣10 mol2•L﹣2,在任何含AgCl固体的溶液中,c(Ag+)=c(Cl﹣)且Ag+与Cl﹣浓度的乘积等于1.8×10﹣10 mol2•L﹣2 |
|
| C. | 温度一定时,当溶液中Ag+和Cl﹣浓度的乘积等于Ksp值时,此溶液为 AgCl的饱和溶液 |
|
| D. | 向饱和AgCl水溶液中加入少量盐酸,Ksp值变大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
根据以下3个热化学方程式:
2H2S(g)+3O2(g)=2SO2(g)+2H2O(l)△H=﹣Q1 kJ/mol
2H2S(g)+O2(g)=2S(s)+2H2O(l)△H=﹣Q2 kJ/mol
2H2S(g)+O2(g)=2S(s)+2H2O(g)△H=﹣Q3 kJ/mol
判断Q1、Q2、Q3三者关系正确的是( )
|
| A. | Q1>Q2>Q3 | B. | Q1>Q3>Q2 | C. | Q3>Q2>Q1 | D. | Q2>Q1>Q3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
铁是人类较早使用的金属之一.运用铁及其化合物的知识,完成下列问题.
(1)所含铁元素既有氧化性又有还原性的物质是 (用字母代号填).
A.Fe; B.FeCl3; C.FeSO4; D.Fe2O3
(2)向沸水中逐滴滴加1 mol/L FeCl3溶液,至液体呈透明的红褐色,该分散系中粒子直径的范围是 nm.
(3)电子工业需要用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,请写出FeCl3溶液与铜反应的离子方程式: .某校同学为测定FeCl3腐蚀铜后所得溶液的组成,进行了如下实验:
首先取少量待测溶液,滴入KSCN溶液呈红色,则溶液中含有的金属阳离子是 ,在此基础上,又进行了定量组成的测定:取50.0mL待测溶液,向其中加入足量的AgNO3溶液,得白色沉淀,过滤、干燥、称量,沉淀质量为43.05g.溶液中c(Cl﹣)= mol/L.
(4)若要验证该溶液中含有Fe2+,正确的实验方法是B.
A.向试管中加入试液,滴入KSCN溶液,若显血红色,证明含有Fe2+;
B.向试管中加入试液,滴入酸性高锰酸钾溶液,若褪色,证明含有Fe2+;
C.向试管中加入试液,滴入氯水,再滴入KSCN溶液,若显血红色,证明原溶液中含有Fe2+.
(5)欲从废水中回收铜,并重新获得FeCl3溶液设计实验方案如下:
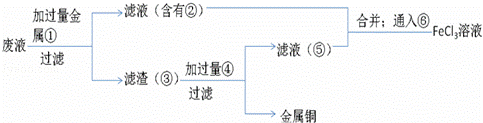
A.请写出上述实验中加入或生成的有关物质的化学式:
① ;② ;③ ;④HCl.
B.请写出通入⑥的化学方程式 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com