
(14分)下表列出了A—R九种元素在周期表中的位置,用元素符号或化学式填空。
 主族 主族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | | | | E | | F | | |
| 3 | A | C | D | | | | G | R |
| 4 | B | | | | | | H | |
(1) Ar; K; KOH; HClO4。 (2) Al(OH)3+OH-=AlO2-+2H2O。(3) K>Na>Mg
(4) 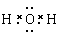 ; HCl>HBr。 (5) NaBr;
; HCl>HBr。 (5) NaBr; 。
。
(6) 离子化合物  ;(7) ⅤA ; MH3。
;(7) ⅤA ; MH3。
解析试题分析:根据元素在周期表中的位置可知:A是Na;B是K;C是Mg;D是Al;E是C;F是O;G是Cl;H是Br;R是Ar。(1)这九种元素中:化学性质最不活泼的是Ar;金属性最强的是K;最高价氧化物的水化物碱性最强的碱是KOH;最高价氧化物的水化物酸性最强的酸是HClO4。(2)Al2O3是两性氧化物,既能与强酸反应产生盐和水,也能与强碱反应产生盐和水。Al2O3与NaOH反应的化学方程式是:Al2O3+2NaOH=2NaAlO2+2H2O,离子方程式是:Al2O3+ 2OH-= 2AlO2-+ H2O。(3)Na、K是同一主族的元素,由于电子层数:K>Na,所以原子半径K>Na;Na、Mg是同一周期的元素。原子序数越大,原子半径就越小。所以原子半径Na>Mg。因此原子半径:K>Na>Mg。(4)F是O,它形成的氢化物H2O是根据化合物,其电子式为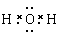 。同一主族的元素,元素的非金属性越强,对应的氢化物的稳定性就越强。由于Cl、Br是同一主族的元素,由于非金属性Cl>Br.所以氢化物的稳定性HCl>HBr。(5)Br元素跟Na元素形成的化合物的化学式是NaBr,Na2O2的电子式是
。同一主族的元素,元素的非金属性越强,对应的氢化物的稳定性就越强。由于Cl、Br是同一主族的元素,由于非金属性Cl>Br.所以氢化物的稳定性HCl>HBr。(5)Br元素跟Na元素形成的化合物的化学式是NaBr,Na2O2的电子式是 .(6)K和O两种元素形成的2:1型化合物K2O属于离子化合物,用电子式表示其形成过程为
.(6)K和O两种元素形成的2:1型化合物K2O属于离子化合物,用电子式表示其形成过程为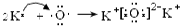 。(7) 按这个规定,第15列元素应为ⅤA ;由于其最外层有5个电子,要达到8的电子的稳定结构少三个电子,所以其简单氢化物的化学式为MH3。
。(7) 按这个规定,第15列元素应为ⅤA ;由于其最外层有5个电子,要达到8的电子的稳定结构少三个电子,所以其简单氢化物的化学式为MH3。
考点:考查元素的推断、元素形成的化合物的结构和性质的比较、电子式表示、化学方程式、了是方程式的书写的知识。


科目:高中化学 来源: 题型:填空题
(12分)【化学—物质结构与性质】
石墨烯(如图甲)是一种由单层碳原子构成的平面结构新型碳材料,石墨烯中部分碳原子被氧化后,其平面结构会发生改变,转化为氧化石墨烯(如图乙).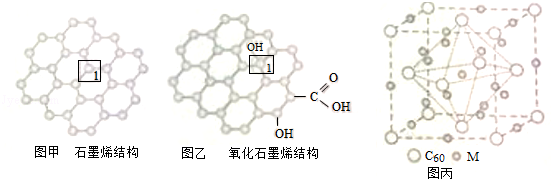
(1)图甲中,1号C与相邻C形成σ键的个数为 _________ .
(2)图乙中,1号C的杂化方式是 _________ ,该C与相邻C形成的键角 _________ (填“>”“<”或“=”)图甲中1号C与相邻C形成的键角.
(3)若将图乙所示的氧化石墨烯分散在H2O中,则氧化石墨烯中可与H2O形成氢键的原子有 _________ (填元素符号).
(4)石墨烯可转化为富勒烯(C60),某金属M与C60可制备一种低温超导材料,晶胞如图丙所示,M原子位于晶胞的棱上与内部,该晶胞中M原子的个数为 _________ ,该材料的化学式为 _________ .
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(15分)【化学—选修3:物质结构与性质】
a、b、c、d、f五种前四周期元素,原子序数依次增大;a、b、c三种元素的基态原子具有相同的能层和能级,第一电离能I1(a)<I1(c)<I1(b),且其中基态b原子的2p轨道处于半充满状态; d为周期表前四周期中电负性最小的元素;f的原子序数为29。请回答下列问题。(如需表示具体元素请用相应的元素符号)
(1)写出ac2的电子式__________;基态f原子的外围电子排布式为 。
(2)写出一种与ac2互为等电子体的物质的化学式 。
(3)b的简单氢化物的沸点比同族元素氢化物的沸点 。(填“高”或“低”)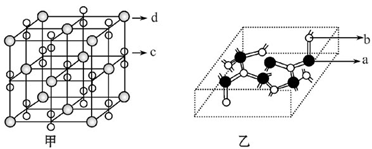
(4)化合物M由c、d两种元素组成,其晶胞结构如甲,则M的化学式为 。
(5)化合物N的部分结构如乙,N由a、b两元素组成,则硬度超过金刚石。试回答:①N的晶体类型为________________________,其硬度超过金刚石的原因是___________________。
②N晶体中a、b两元素原子的杂化方式均为___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(15分)已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数依次增加。相关信息如下表所示,根据推断回答下列问题:(答题时A、B、C、D、E用所对应的元素符号表示)
| A | A的最高价氧化物对应的水化物化学式为H2AO3 |
| B | B元素的第一电离能比同周期相邻两个元素都大 |
| C | C原子在同周期原子中半径最大(稀有气体除外),其单质焰色为黄色 |
| D | Z的基态原子最外层电子排布式为3s23p2 |
| E | E与C位于不同周期,E原子核外最外层电子数与C相同,其余各层电子均充满 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(1)元素的第一电离能Al Si(填“>”或“<”)。
(2)基态Mn2+的核外电子排布式为 。
(3)硅烷(SinH2n+2)的沸点与其相对分子质量的变化关系如图所示,呈现这种变化关系的原因是 。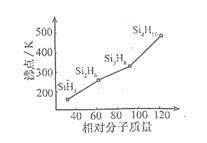
(4)硼砂是含结晶水的四硼酸钠,其阴离子Xm-(含B、O、H三种元素)的球棍模型如图所示: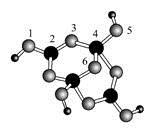
①在Xm-中,硼原子轨道的杂化类型有 ;配位键存在于 原子之间(填原子的数字标号);m= (填数字)。
②硼砂晶体由Na+、Xm-和H2O构成,它们之间存在的作用力有 (填序号)。
A、离子键 B、共价键 C、金属键 D、范德华力 E、氢键
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,回答下列问题: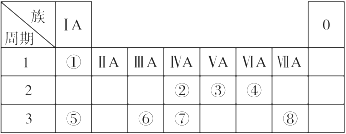
(1)在以上元素的原子中,原子半径最大的是 (填元素符号)。
(2)地壳中含量居于第二位的元素在周期表中的位置是 。
(3)①、④、⑤中的某些元素可形成既含离子键又含共价键的离子化合物,写出两种化合物的电子式 、 。
(4)W是第四周期与④同主族的元素。据此推测W不可能具有的性质是 。
| A.最高正化合价为+6价 | B.气态氢化物比H2S稳定 |
| C.最高价氧化物的水化物的酸性比硫酸弱 | D.单质在常温下可与氢气化合 |

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(14分)下表为元素周期表的一部分:
 族 族周期 | | | | |||||
| 1 | ① | | | | | | | |
| 2 | | | | | | ② | | |
| 3 | ③ | | | ④ | | ⑤ | ⑥ | |
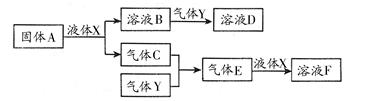
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
下表为元素周期表的一部分:
| 族 周期 | | | | |||||
| 1 | ① | | | | | | | |
| 2 | | | | | | ② | | |
| 3 | ③ | | | ④ | | ⑤ | ⑥ | |
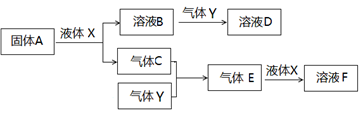
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
氮可以形成多种离子,如N3-、N3-、NH2-、NH4+、N2H5+、N2H62+等,已知N2H5+与N2H62+是由中性分子X结合H+形成的,有类似于NH4+的性质。
⑴ 1个N3-离子含有 个电子;
⑵ 形成N2H5+离子的中性分子X的分子式是 ;
X在氧气中可以燃烧,写出燃烧反应的化学方程式 ;
⑶ 写出N2H62+离子在强碱溶液中反应的离子方程式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com