
【题目】向Ba(OH)2溶液中逐滴加入稀硫酸,请完成下列问题:
(1)写出反应的离子方程式:__。
(2)下列三种情况下,离子方程式与(1)相同的是__(填字母)。
A.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至溶液显中性
B.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至![]() 恰好完全沉淀
恰好完全沉淀
C.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至过量
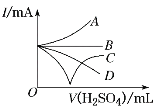
(3)若缓缓加入稀硫酸直至过量,整个过程中混合溶液的导电能力(用电流强度I表示)可近似地用图中的__曲线表示(填字母)。
(4)化合物高铁酸钾K2FeO4可作为一种“绿色高效多功能”的水处理剂,可由FeCl3和KClO在强碱条件下反应制得,该反应的离子方程式为__(反应物写Fe3+)。
【答案】Ba2++2OH-+![]() +2H+=BaSO4↓+2H2O A C 2Fe3++3ClO-+10OH- =2
+2H+=BaSO4↓+2H2O A C 2Fe3++3ClO-+10OH- =2![]() +3Cl-+5H2O
+3Cl-+5H2O
【解析】
书写反应的离子方程式时,遵循“以少定多”的原则,即可假设少量的物质为1mol,则另一物质过量,过量的物质,用量需要多少,就能提供多少。
(1)向Ba(OH)2溶液中逐滴加入稀硫酸,发生反应的化学方程式为Ba(OH)2+ H2SO4= BaSO4↓+ 2H2O,反应的离子方程式:Ba2++2OH-+![]() +2H+=BaSO4↓+2H2O。答案为:Ba2++2OH-+
+2H+=BaSO4↓+2H2O。答案为:Ba2++2OH-+![]() +2H+=BaSO4↓+2H2O;
+2H+=BaSO4↓+2H2O;
(2) A.设NaHSO4为1mol,则n(H+)=1mol,n(![]() )=1mol,逐滴加入Ba(OH)2溶液至溶液显中性,需n(OH-)=1mol,应投入n[Ba(OH)2]=0.5mol,离子方程式为Ba2++2OH-+
)=1mol,逐滴加入Ba(OH)2溶液至溶液显中性,需n(OH-)=1mol,应投入n[Ba(OH)2]=0.5mol,离子方程式为Ba2++2OH-+![]() +2H+=BaSO4↓+2H2O,A符合题意;
+2H+=BaSO4↓+2H2O,A符合题意;
B.设NaHSO4为1mol,则n(H+)=1mol,n(![]() )=1mol,逐滴加入Ba(OH)2溶液至
)=1mol,逐滴加入Ba(OH)2溶液至![]() 恰好完全沉淀,应投入n[Ba(OH)2]=1mol,有1molOH-参加反应,1molOH-剩余,离子方程式为Ba2++OH-+
恰好完全沉淀,应投入n[Ba(OH)2]=1mol,有1molOH-参加反应,1molOH-剩余,离子方程式为Ba2++OH-+![]() +H+=BaSO4↓+H2O,B不合题意;
+H+=BaSO4↓+H2O,B不合题意;
C.设NaHSO4为1mol,则n(H+)=1mol,n(![]() )=1mol,逐滴加入Ba(OH)2溶液至过量,则需消耗n(OH-)=1mol,n(Ba2+)=1mol,离子方程式为Ba2++OH-+
)=1mol,逐滴加入Ba(OH)2溶液至过量,则需消耗n(OH-)=1mol,n(Ba2+)=1mol,离子方程式为Ba2++OH-+![]() +H+=BaSO4↓+H2O,C不合题意;
+H+=BaSO4↓+H2O,C不合题意;
故答案为:A;
(3) 向Ba(OH)2溶液中缓缓加入稀硫酸直至过量,发生反应为Ba2++2OH-+![]() +2H+=BaSO4↓+2H2O,过量的硫酸发生电离H2SO4=2H++
+2H+=BaSO4↓+2H2O,过量的硫酸发生电离H2SO4=2H++![]() 。起初溶液中离子浓度逐渐减小,刚好完全反应时,离子浓度接近0;硫酸过量以后,发生电离,使溶液的导电能力不断增大,最后保持恒定,所以导电能力先减小到接近0,后逐渐增大到一定程度,然后保持不变,故答案为:C;
。起初溶液中离子浓度逐渐减小,刚好完全反应时,离子浓度接近0;硫酸过量以后,发生电离,使溶液的导电能力不断增大,最后保持恒定,所以导电能力先减小到接近0,后逐渐增大到一定程度,然后保持不变,故答案为:C;
(4)FeCl3和KClO在强碱条件下发生氧化还原反应,生成![]() 、Cl-等,根据得失电子守恒、原子守恒和电荷守恒,该反应的离子方程式为2Fe3++3ClO-+10OH- =2
、Cl-等,根据得失电子守恒、原子守恒和电荷守恒,该反应的离子方程式为2Fe3++3ClO-+10OH- =2![]() +3Cl-+5H2O。答案为:2Fe3++3ClO-+10OH- =2
+3Cl-+5H2O。答案为:2Fe3++3ClO-+10OH- =2![]() +3Cl-+5H2O。
+3Cl-+5H2O。


科目:高中化学 来源: 题型:
【题目】下列关于有机物的说法正确的是
A.乙烯、苯、油脂中都含有碳碳双键
B.按系统命名法,有机物![]() 的名称是
的名称是![]() 甲基
甲基![]() 丙烯
丙烯
C.乙烯使溴水、酸性高锰酸钾溶液褪色的反应原理相同
D.![]() 有8种同分异构体,它们的熔、沸点各不相同
有8种同分异构体,它们的熔、沸点各不相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Li是最轻的固体金属,采用Li作为负极材料的电池具有小而轻、能量密度大等优良性能,得到广泛应用。回答下列问题:
(1)下列Li原子电子排布图表示的状态中,能量最低和最高的分别为___、___(填标号)。
A.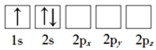
B.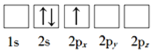
C.![]()
D.![]()
(2)Li+与H具有相同的电子构型,r(Li+)小于r(H),原因是___。
(3)LiAlH4是有机合成中常用的还原剂,LiAlH4中的阴离子(AlH![]() )空间构型是___、中心原子的杂化形式为___。
)空间构型是___、中心原子的杂化形式为___。
(4)Li2O是离子晶体,其晶格能可通过如图的BornHaber循环计算得到。
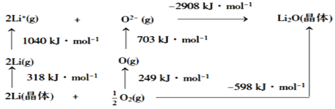
可知,Li原子的第一电离能为___kJ·mol1,O=O键键能为___kJ·mol1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在探究新制饱和氯水成分的实验中,下列实验现象或结论不正确的是( )
A.氯水的颜色呈浅黄绿色,说明氯水中含有Cl2
B.向氯水中滴加硝酸酸化的AgNO3溶液,产生白色沉淀,说明氯水中含有Cl-
C.向氯水中加入NaHCO3粉末,有气泡产生,说明氯水中含有H+
D.向氯水中滴加紫色石蕊,溶液颜色变成红色,说明氯水中含有HClO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)0.5mol·L-1MgCl2溶液中c(Cl-)为___mol·L-1,从100mL该溶液中取出20mL再稀释至100mL,c(MgCl2)为__mol·L-1。
(2)将SO2通入氯化钡溶液中无现象;若将SO2通入硝酸钡溶液中有白色沉淀产生,其化学反应方程式如下(未配平):SO2+Ba(NO3)2+H2O→BaSO4↓+HNO3+NO↑。
①配平上述化学反应方程式并用双线桥表示电子转移的方向和数目___。
②该反应中,__元素发生氧化反应,氧化剂是__(写化学式)。氧化产物与还原产物的物质的量之比为___。
③当反应消耗19.2gSO2时,反应中转移电子__mol,在标准状况下,生成NO的体积为__L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个绝热的固定容积的密闭容器中,发生可逆反应mA(g)+nB(g)![]() pC(g)+qD(s),当m、n、p、q为任意整数时,一定可以作为反应达到平衡的标志是( )
pC(g)+qD(s),当m、n、p、q为任意整数时,一定可以作为反应达到平衡的标志是( )
①体系的压强不再改变 ②体系的温度不再改变 ③体系的密度不再变化 ④各组分质量分数不再改变
A.①②③B.①②③④C.②③④D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据如图所示实验装置,回答下列问题。
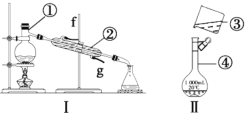
(1)写出下列仪器的名称:①___,④___。
(2)仪器①~④中,使用时必须检查是否漏水的是___(填序号)。
(3)若利用装置Ⅰ分离酒精和水的混合物,还缺少的仪器是___,②的进水口是__(填“f”或“g”)。
(4)配制溶液时,下列操作会导致所配溶液的浓度偏低的是__(填标号)。
a.洗涤烧杯和玻璃棒的溶液未转移入容量瓶中
b.定容时,眼睛俯视使溶液凹面最低点与容量瓶刻度线相切
c.容量瓶中原残留有少量蒸馏水
d.定容后加水过量,又从容量瓶中取出部分溶液,使液面降至刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在某密闭容器中发生反应:2HI(g)![]() H2(g)+I2(s) ΔH>0,若0~15s内c(HI)由0.1mol·L-1降到0.07mol·L-1,则下列说法正确的是( )
H2(g)+I2(s) ΔH>0,若0~15s内c(HI)由0.1mol·L-1降到0.07mol·L-1,则下列说法正确的是( )
A.0~15s内用I2的平均反应速率为v(I2)=0.001mol·L-1·s-1
B.c(HI)由0.07mol·L-1降到0.05mol·L-1所需的反应时间为小于10s
C.升高温度正反应速率加快,逆反应速率减慢
D.减小反应体系的体积,化学反应速率加快
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】香草醛又名香兰素,是食品和药品的重要原料,其结构简式如图所示。下列有关香草醛的说法中不正确的是( )

A.香草醛可以发生银镜反应
B.在一定条件下1mol香草醛可以与4molH2反应
C.香草醛遇FeCl3溶液可变色
D.香草醛可与NaOH溶液反应,也可与NaHCO3溶液反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com