
| A. | 电解饱和NaOH溶液时溶液的pH变大 | |
| B. | 在镀件上电镀铜时,可以不用金属铜做阳极,只要溶液中存在Cu2+就可以 | |
| C. | 电解稀硫酸制O2、H2时,铜做阳极 | |
| D. | 铝-空气燃料电池通常以NaOH溶液为电解液,电池在工作过程中电解液的pH保持不变 |
分析 A.电解饱和NaOH溶液就是电解水;
B.电镀时阴极上铜离子得电子生成Cu;
C.活性电极作阳极上电极失电子;
D.铝空气燃料电池以NaOH溶液为电解液中负极反应为Al+4OH---3e-═AlO2-+2H2O,正极反应为O2+2H2O+4e-=4OH-,总反应为4Al+4OH-+3O2═4AlO2-+2H2O.
解答 解:A.电解饱和NaOH溶液,阴极上氢离子得电子,阳极上氢氧根离子失电子,所以是电解水,会有氢氧化钠析出,由于饱和溶液的浓度只与温度有关,温度不变,氢氧化钠的浓度不变,所以pH不变,故A错误;
B.在镀件上电镀铜时,待镀金属作阴极,阴极上铜离子得电子生成Cu,只要溶液中存在足够的Cu2+就可以在镀件上镀铜,所以可以不用金属铜做阳极,故B正确;
C.活性电极作阳极上电极失电子,电解稀硫酸制O2、H2时,若铜做阳极,则Cu失电子生成铜离子,溶液中的阴离子不能失电子,所以得不到氧气,故C错误;
D.铝空气燃料电池以NaOH溶液为电解液中负极反应为Al+4OH---3e-═AlO2-+2H2O,正极反应为O2+2H2O+4e-=4OH-,总反应为4Al+4OH-+3O2═4AlO2-+2H2O,该电池在放电时消耗了碱,溶液pH降低,故D错误.
故选B.
点评 本题考查了原电池原理的应用,题目难度不大,侧重于基础知识的应用的考查,注意把握溶液中离子的放电顺序以及电极方程式的书写方法.


科目:高中化学 来源: 题型:解答题
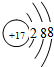 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C2H4O | B. | C2H5OH | C. | CH3CHO | D. | CH3COOH |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
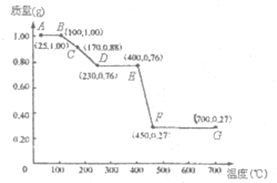 如图是1.00g MgC2O4•nH2O晶体放在坩埚里从25℃徐徐加热至700℃时,所得同体产物的质量(m)随温度(t)变化的关系曲线.(已知100℃以上才会逐渐失去结晶水,并约在230℃时完全失去结晶水)
如图是1.00g MgC2O4•nH2O晶体放在坩埚里从25℃徐徐加热至700℃时,所得同体产物的质量(m)随温度(t)变化的关系曲线.(已知100℃以上才会逐渐失去结晶水,并约在230℃时完全失去结晶水)查看答案和解析>>
科目:高中化学 来源: 题型:解答题

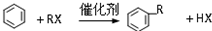 A具有和苯相似的性质.
A具有和苯相似的性质. 2HCHO+2H2O;
2HCHO+2H2O;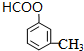 、
、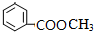 ;
;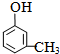 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 配制5%的食盐溶液时,将称量的食盐放在烧杯中加适量的蒸馏水搅拌溶解 | |
| B. | 用酸式滴定管准确量取10.00 mL KMnO4溶液 | |
| C. | 用500 mL容量瓶配制1 mol/L的NaOH溶液 | |
| D. | 用pH试纸测得新制氯水的pH为2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
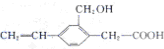
| A. | 该有机化合物的分子式为C11H10O3 | |
| B. | 该有机化合物能发生取代反应、加成反应和加聚反应 | |
| C. | 1mol该有机化合物分别消耗Na、NaOH和NaHCO3的物质的量之比为2:2:1 | |
| D. | 该有机化合物与 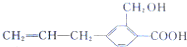 互为同系物 互为同系物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用惰性电极电解饱和食盐水时,阳极的电极反应式为:2Cl--2e-═Cl2↑ | |
| B. | 向沸水中滴加FeCl3饱和溶液制备Fe(OH)3胶体:Fe3++3H2O$\frac{\underline{\;\;△\;\;}}{\;}$ Fe(OH)3↓+3H+ | |
| C. | 粗铜精炼时,与电源正极相连的是纯铜,正极反应式为:Cu-2e-═Cu2+ | |
| D. | NaHS水解:HS-+H2O?H3O++S2- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某废金属屑中主要成分为Cu、Fe、Al,还含有少量的铜锈[Cu2(OH)2CO3]、少量的铁锈和少量的氧化铝,用上述废金属屑制取胆矾(CuSO4•5H2O)、无水AlCl3和铁红的过程如图所示:
某废金属屑中主要成分为Cu、Fe、Al,还含有少量的铜锈[Cu2(OH)2CO3]、少量的铁锈和少量的氧化铝,用上述废金属屑制取胆矾(CuSO4•5H2O)、无水AlCl3和铁红的过程如图所示:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com