
 .
.分析 (1)有机物中含有双键能发生聚合反应;
(2)根据有机物A蒸气密度是相同状况下甲烷密度的6.25倍,可以计算其相对分子质量,根据元素的质量分数可以计算原子个数比,得到最简式.
解答 解:(1)丙烯中含有双键能发生聚合反应,反应方程式为: ,故答案为:
,故答案为: ;
;
(2)元素的质量分数为:碳60%、氧32%,则原子个数之比:C:O:H=$\frac{60%}{12}$:$\frac{32%}{16}$:$\frac{8%}{1}$=5:2:8,有机物A蒸气密度是相同状况下甲烷密度的6.25倍,可以计算其相对分子质量为:16×6.25=100,分子式为:C5H8O2,故答案为:C5H8O2.
点评 本题考查学生有机物的分子式的确定以及有机物的方程式的书写知识,难度不大,注意基础知识的积累.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
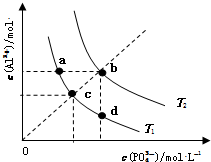
| A. | 图象中四个点的Ksp:a=b>c>d | B. | AlPO4在b点对应的溶解度大于c点 | ||
| C. | AlPO4(s)→Al3+(aq)+PO43-(aq)△H<0 | D. | 升高温度可使d点移动到b点 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验室中用含有Ca2+、Mg2+、Cl-的自来水制取蒸馏水,可采用蒸馏的方法 | |
| B. | 用CCl4萃取碘水的实验中,振荡静置后,上层为紫红色溶液 | |
| C. | 利用植物油的密度比水小的原理,可用分液的方法分离这两种液体混合物 | |
| D. | 蒸馏时,温度计的水银球应充分接触溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
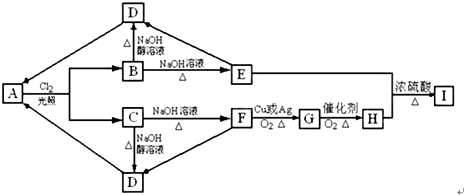
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 胶体与溶液的本质区别是分散质颗粒的大小不同 | |
| B. | 氯化铁溶液可应急止血,利用的是胶体的聚沉 | |
| C. | 溶液是电中性的,胶体是带电的 | |
| D. | 将稀硫酸逐滴加入氢氧化铁胶体中,开始时产生沉淀,继续滴加时沉淀又溶解 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 两个反应中NaHSO4均为氧化产物 | |
| B. | 碘元素在反应①中被还原,在反应②中被氧化 | |
| C. | 氧化性:MnO2>SO${\;}_{4}^{2-}$>IO${\;}_{3}^{-}$>I2 | |
| D. | 反应①、②中生成等量的I2时转移电子数比为1:5 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | Na+、Ag+、Cl-、CO32- | B. | H+、Na+、Fe2+、MnO4- | ||
| C. | K+、Ca2+、Cl-、NO3- | D. | K+、NH4+、OH-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com