
”¾ĢāÄæ”æ(1)ŌŚ25 ”ę”¢101 kPaµÄĢõ¼žĻĀ£¬

Ēė»Ų“šĻĀĮŠÓŠ¹ŲĪŹĢā£ŗ
¢ŁÓÉH£«H”śH2£¬µ±Éś³É1 mol H2Ź±£¬ŅŖ________(Ģī”°ĪüŹÕ”±»ņ”°·Å³ö”±£¬ĻĀĶ¬)436 kJµÄÄÜĮ棻ÓÉCl2”śCl£«Cl£¬µ±¶ĻĮŃ1 mol Cl2ÖŠµÄ¹²¼Ū¼üŹ±£¬ŅŖ________243 kJµÄÄÜĮ攣
¢Ś¶ŌÓŚ·“Ó¦H2(g)£«Cl2(g)=2HCl(g)£¬²āµĆÉś³É2 molHCl(g)Ź±£¬·“Ó¦¹ż³ĢÖŠ·Å³ö183 kJµÄČČĮ棬Ōņ¶ĻæŖ 1 mol H”ŖCl ¼üĖłŠčµÄÄÜĮæŹĒ________kJ”£
¢ŪÓŠĮ½øö·“Ó¦£ŗa.H2(g)£«Cl2(g)![]() 2HCl(g)£¬b.H2(g)£«Cl2(g)
2HCl(g)£¬b.H2(g)£«Cl2(g)![]() 2HCl(g)”£ÕāĮ½øö·“Ó¦ÖŠ£¬ĻąĶ¬ĪļÖŹµÄĮæµÄH2(g)”¢Cl2(g)·“Ӧɜ³ÉĻąĶ¬ÖŹĮæµÄHCl(g)Ź±£¬·Å³öµÄÄÜĮæ________(Ģī”°ĻąµČ”±»ņ”°²»ĻąµČ”±)”£
2HCl(g)”£ÕāĮ½øö·“Ó¦ÖŠ£¬ĻąĶ¬ĪļÖŹµÄĮæµÄH2(g)”¢Cl2(g)·“Ӧɜ³ÉĻąĶ¬ÖŹĮæµÄHCl(g)Ź±£¬·Å³öµÄÄÜĮæ________(Ģī”°ĻąµČ”±»ņ”°²»ĻąµČ”±)”£
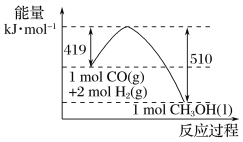
(2)øł¾ŻĶ¼Ź¾µÄÄÜĮæ×Ŗ»Æ¹ŲĻµÅŠ¶Ļ£¬Éś³É16 g CH3OH(l)________(Ģī”°ĪüŹÕ”±»ņ”°·Å³ö”±)________kJÄÜĮ攣
”¾“š°ø”æ·Å³ö ĪüŹÕ 431 ĻąµČ ·Å³ö 45.5
”¾½āĪö”æ
(1)¢Ł¶ĻæŖ½ØĪüŹÕÄÜĮ棬³É¼üŠčŅŖŹĶ·ÅÄÜĮ棻
¢Śøł¾ŻģŹ±ä=·“Ó¦Īļ×ܼüÄÜ-Éś³ÉĪļ×ܼüÄÜ£»
¢Ūøł¾ŻøĒĖ¹¶ØĀÉ£¬·“Ó¦ČČÓė·“Ó¦Ģõ¼žĪŽ¹Ų£¬Ö»ÓėŹ¼Ģ¬ŗĶÖÕĢ¬ÓŠ¹Ų£»
(2)øł¾ŻĶ¼Ź¾£¬·“Ó¦Īļ×ÜÄÜĮæøßÓŚÉś³ÉĪļ×ÜÄÜĮ棬·“Ó¦·Å³ö»ņĪüŹÕµÄÄÜĮæÓė²ĪÓė·“Ó¦µÄĪļÖŹµÄĪļÖŹµÄĮæ³ÉÕż±Č”£
(1)¢Ł¶ĻæŖ½ØĪüŹÕÄÜĮ棬³É¼üŠčŅŖŹĶ·ÅÄÜĮ棬ÓÉH£«H”śH2£¬ŹĒ³É¼ü¹ż³Ģ£¬ŹĶ·ÅÄÜĮ棬µ±Éś³É1 mol H2Ź±£¬ŅŖ·Å³ö436 kJµÄÄÜĮ棻ÓÉCl2”śCl£«Cl£¬ŹĒ¶Ļ¼ü¹ż³Ģ£¬¶Ļ¼üĪüŹÕÄÜĮ棬µ±¶ĻĮŃ1 mol Cl2ÖŠµÄ¹²¼Ū¼üŹ±£¬ŅŖĪüŹÕ243 kJµÄÄÜĮ棻
¢Śøł¾ŻģŹ±ä=·“Ó¦Īļ×ܼüÄÜ-Éś³ÉĪļ×ܼüÄÜ£¬¶ĻĮŃ1molH-H¼üÓė1molCl-Cl¼üĪüŹÕµÄÄÜĮæÖ®ŗĶ£¬¼“436kJ+243kJ=679kJ£¬Éč¶ĻæŖ1molH-Cl¼üĪüŹÕµÄ×ÜÄÜĮæĪŖE(H-Cl)£¬ŌņÓŠ( 436kJ+243kJ) -2”ĮE(H-Cl) =-183kJ£¬ŌņE(H-Cl)=431kJ£»
¢ŪĮ½øö·“Ó¦µÄÄÜĮæ×Ŗ»ÆŠĪŹ½Ö÷ŅŖŹĒ»ÆѧÄÜ×Ŗ»ÆĪŖČČÄÜ£¬Ņ»øö¾ßĢåµÄ·“Ó¦ŹĶ·ÅÄÜĮæµÄ¶ąÉŁÓė·“Ó¦Ģõ¼žĪŽ¹Ų£¬¶ųÓė¶ĻæŖ¾É»Æѧ¼üŗĶŠĪ³ÉŠĀ»Æѧ¼üµÄÄÜĮæ±ä»ÆÓŠ¹Ų£¬ĖłŅŌÉś³ÉµČĮæµÄ²śĪļĖłŹĶ·ÅµÄÄÜĮæĻąµČ£»
(2)øł¾ŻĶ¼Ź¾±ä»ÆæÉÖŖ£¬·“Ó¦Īļ×ÜÄÜĮæøßÓŚÉś³ÉĪļ×ÜÄÜĮ棬øĆ·“Ó¦ŹōÓŚŹĶ·ÅÄÜĮæµÄ·“Ó¦£¬Éś³É1mol CH3OH(l)·Å³öµÄÄÜĮæĪŖ510kJ-419kJ=91kJ£¬16gCH3OHµÄĪļÖŹµÄĮæĪŖ0.5mol£¬¹ŹÉś³É16g CH3OH(l)·Å³öµÄČČĮæĪŖ45.5kJ”£


 ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø
ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚ²»Ķ¬Ģõ¼žĻĀ·Ö±š²āµĆ·“Ó¦2SO2+O2![]() 2SO3µÄ»Æѧ·“Ó¦ĖŁĀŹ£¬ĘäÖŠ±ķŹ¾øĆ·“Ó¦½ųŠŠ×īæģµÄŹĒ£Ø £©
2SO3µÄ»Æѧ·“Ó¦ĖŁĀŹ£¬ĘäÖŠ±ķŹ¾øĆ·“Ó¦½ųŠŠ×īæģµÄŹĒ£Ø £©
A. v(SO2)£½4 mol”¤L-1”¤min-1B. v (O2)£½3 mol”¤L-1”¤min-1
C. v (SO3)="0.1" mol”¤L-1”¤s-1D. v (O2)£½0.1mol”¤L-1”¤s-1
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĶ¼ŹĒŹµŃéŹŅÖĘČ”SO 2²¢ŃéÖ¤SO 2µÄijŠ©ŠŌÖŹµÄ×°ÖĆ£¬Ēė»Ų“š£ŗ
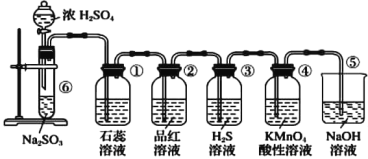
(1)ŌŚ¢ŽÖŠ·¢Éś·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ_____________________”£
(2)¢ŁÖŠµÄŹµŃéĻÖĻóĪŖŹÆČļČÜŅŗ__________£¬“ĖŹµŃéÖ¤Ć÷SO 2¾ßÓŠ_________µÄŠŌÖŹ”£
(3)¢ŚÖŠµÄĘ·ŗģČÜŅŗ________”£
(4)¢ŪÖŠ·¢ÉśµÄ»Æѧ·“Ó¦·½³ĢŹ½ĪŖ________________”£
(5)¢ÜÖŠµÄŹµŃéĻÖĻóŹĒ______________________£¬Ö¤Ć÷SO 2ÓŠ_____________ŠŌ”£
(6)¢Ż×°ÖƵÄ×÷ÓĆŹĒ_________£¬øĆ·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ·“Ó¦¢ń£ŗCaSO4(s)£« CO(g) ![]() CaO(s)£«SO2(g)£«CO2(g)”” ¦¤H£½£«218.4 kJ”¤mol£1·“Ó¦¢ņ£ŗCaSO4(s)£«4CO(g)
CaO(s)£«SO2(g)£«CO2(g)”” ¦¤H£½£«218.4 kJ”¤mol£1·“Ó¦¢ņ£ŗCaSO4(s)£«4CO(g) ![]() CaS(s)£«4CO2(g) ¦¤H£½£175.6 kJ”¤mol£1¼ŁÉčijĪĀ¶ČĻĀ£¬·“Ó¦¢ńµÄĖŁĀŹ(v1)“óÓŚ·“Ó¦¢ņµÄĖŁĀŹ(v2)£¬ŌņĻĀĮŠ·“Ó¦¹ż³ĢÄÜĮæ±ä»ÆŹ¾ŅāĶ¼ÕżČ·µÄŹĒ
CaS(s)£«4CO2(g) ¦¤H£½£175.6 kJ”¤mol£1¼ŁÉčijĪĀ¶ČĻĀ£¬·“Ó¦¢ńµÄĖŁĀŹ(v1)“óÓŚ·“Ó¦¢ņµÄĖŁĀŹ(v2)£¬ŌņĻĀĮŠ·“Ó¦¹ż³ĢÄÜĮæ±ä»ÆŹ¾ŅāĶ¼ÕżČ·µÄŹĒ
A.  B.
B. 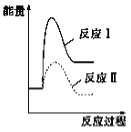 C.
C.  D.
D. 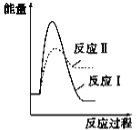
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÓĆĻĀĮŠŹµŃé×°ÖĆ£Ø²æ·Ö¼Š³Ö×°ÖĆĀŌČ„£©½ųŠŠĻąÓ¦µÄŹµŃ飬ÄÜ“ļµ½ŹµŃéÄæµÄµÄŹĒ £Ø £©
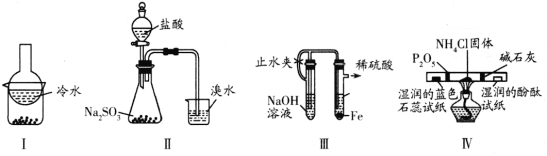
A. ¼ÓČČ×°ÖĆIÖŠµÄÉÕ±·ÖĄėI2ŗĶøßĆĢĖį¼Ų¹ĢĢå
B. ÓĆ×°ÖĆIIŃéÖ¤¶žŃõ»ÆĮņµÄĘư׊Ō
C. ÓĆ×°ÖĆIIIÖʱøĒāŃõ»ÆŃĒĢś³Įµķ
D. ÓĆ×°ÖĆIV¼ģŃéĀČ»Æļ§ŹÜČČ·Ö½āÉś³ÉµÄĮ½ÖÖĘųĢå
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŠĀŠĶŠæµāŅŗĮ÷µē³Ų¾ßÓŠÄÜĮæĆܶČøß”¢Ń»·ŹŁĆü³¤µČÓÅŹĘ£¬Ę乤×÷ŌĄķČēĶ¼ĖłŹ¾”£ĻĀĮŠĖµ·Ø“ķĪóµÄŹĒ

A. ·ÅµēŹ±µēĮ÷“ÓŹÆÄ«µē¼«Į÷ĻņŠæµē¼«
B. ³äµēŹ±Ńō¼«·“Ó¦Ź½ĪŖ£ŗ3I££2e££½I3£
C. Čō½«ŃōĄė×Ó½»»»Ä¤»»³ÉŅõĄė×Ó½»»»Ä¤£¬·ÅµēŹ±Õżøŗ¼«Ņ²ĖęÖ®øıä
D. ·ÅµēŹ±×ó²ąµē½āÖŹ“¢¹ŽÖŠµÄĄė×Ó×ÜÅضČŌö“ó
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚ25”ꏱ£¬FeSµÄKsp£½6.3”Į10£18£¬CuSµÄKsp£½1.3”Į10£36£¬ZnSµÄKsp£½1.3”Į10£24”£ĻĀĮŠÓŠ¹ŲĖµ·ØÖŠÕżČ·µÄŹĒ
A. ±„ŗĶCuSČÜŅŗÖŠCu2£«µÄÅضČĪŖ1.3”Į10£36 mol”¤L£1
B. 25”ꏱ£¬FeSµÄČܽā¶Č“óÓŚCuSµÄČܽā¶Č
C. ĻņĪļÖŹµÄĮæÅضČĻąĶ¬µÄFeCl2”¢ZnCl2µÄ»ģŗĻŅŗÖŠ¼ÓČėÉŁĮæNa2S£¬Ö»ÓŠFeS³ĮµķÉś³É
D. Ļņ±„ŗĶZnSČÜŅŗÖŠ¼ÓČėÉŁĮæZnCl2¹ĢĢ壬ZnSµÄKsp±ä“ó
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”涬¼¾ĪŅ¹ś±±·½“ó²æ·ÖµŲĒų³öĻÖĪķö²ĢģĘų£¬ŅżĘšĪķö²µÄĪ¢ĻøĮ£×Ó°üŗ¬(NH4)2SO4”¢NH4NO3”¢ÓŠ»śæÅĮ£Īļ”¢Ńļ³¾”¢ÖŲ½šŹōĶµČ”£
£Ø1£©NŌŖĖŲŌ×ÓŗĖĶāµē×ÓŌʵĊĪדӊ___ÖÖ£»»łĢ¬ĶŌ×ӵļŪµē×ÓÅŲ¼Ź½ĪŖ___”£
£Ø2£©NŗĶOÖŠµŚŅ»µēĄėÄܽĻŠ”µÄŌŖĖŲŹĒ__£»SO42-µÄæռ乹ŠĶ___”£
£Ø3£©Īķö²ÖŠŗ¬ÓŠÉŁĮæµÄĖ®£¬×é³ÉĖ®µÄĒāŌŖĖŲŗĶŃõŌŖĖŲŅ²ÄÜŠĪ³É»ÆŗĻĪļH2O2£¬ĘäÖŠŠÄŌ×ÓµÄŌӻƹģµĄĄąŠĶĪŖ___£¬H2O2ÄŃČÜÓŚCC14£¬ĘäŌŅņĪŖ___”£
£Ø4£©PM2.5ø»ŗ¬NO£¬NOÄܱ»FeSO4ČÜŅŗĪüŹÕÉś³ÉÅäŗĻĪļ[Fe(NO)(H2O)5]SO4£¬øĆÅäŗĻĪļÖŠŠÄĄė×ÓµÄÅäĪ»ŹżĪŖ___”£
£Ø5£©²ā¶Ø“óĘųÖŠPM2.5ÅØ¶ČµÄ·½·ØÖ®Ņ»ŹĒ¦Ā-ÉäĻßĪüŹÕ·Ø£¬¦Ā-ÉäĻß·ÅÉäŌ“æÉÓĆ85Kr”£ŅŃÖŖKr¾§ĢåµÄ¾§°ū½į¹¹ČēĶ¼ĖłŹ¾£¬ÉčNAĪŖ°¢·ü¼ÓµĀĀŽ³£ŹżµÄÖµ£¬¾§°ū±ß³¤ĪŖ540pm£¬ŌņøĆ¾§ĢåµÄĆÜ__g/cm3(Ö»ĮŠŹ½²»¼ĘĖć£¬KrĦ¶ūÖŹĮæĪŖ84g”¤mol-1)”£
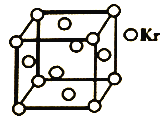
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æČÜŅŗ AÖŠæÉÄÜŗ¬ÓŠČēĻĀĄė×Ó£ŗNa+”¢NH4+”¢Ba2+”¢Mg2+”¢SO42£”¢SO32£”¢Cl£”¢OH£”£Ä³Ķ¬Ń§Éč¼Ę²¢Ķź³ÉĮĖČēĻĀµÄŹµŃé£ŗ
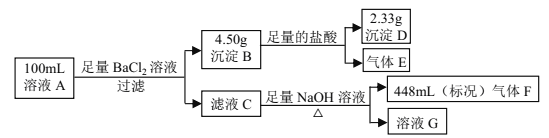
ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A. ČÜŅŗ A ÖŠŅ»¶Ø“ęŌŚ NH4+”¢ SO42£”¢ SO32££¬æÉÄÜ“ęŌŚ Na+
B. ČÜŅŗ A ÖŠŅ»¶Ø“ęŌŚ NH4+”¢ Mg2+”¢ SO42£”¢ SO32££¬æÉÄÜ“ęŌŚ Cl£
C. ČÜŅŗ A ÖŠæÉÄÜ“ęŌŚ Cl££¬ĒŅ c(Na+) ”Ż 0.20 mol”¤L-1
D. Čē¹ūĘųĢå F ÄÜŹ¹ŹŖČóµÄĄ¶É«ŹÆČļŹŌÖ½±äŗģ£¬ĖµĆ÷ČÜŅŗÖŠŅ»¶Øŗ¬ÓŠ NH4+
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com