
 2NH3(g) ��H��0����Ӧ��NH3�����ʵ���Ũ�ȵı仯���������ͼ��ʾ��
2NH3(g) ��H��0����Ӧ��NH3�����ʵ���Ũ�ȵı仯���������ͼ��ʾ�� 
 ��ĩ���䵥Ԫ�����ิϰ��ϵ�д�
��ĩ���䵥Ԫ�����ิϰ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
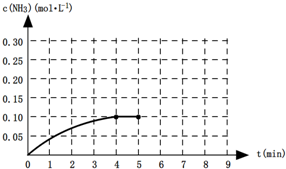
 һ���¶��£���һ2L�ĺ����ܱ������ڼ���0.2molN2��0.6mol H2���������·�Ӧ��N2��g��+3H2��g��?2NH3��g����H��0����Ӧ��NH3�����ʵ���Ũ�ȵı仯�������ͼ��ʾ��
һ���¶��£���һ2L�ĺ����ܱ������ڼ���0.2molN2��0.6mol H2���������·�Ӧ��N2��g��+3H2��g��?2NH3��g����H��0����Ӧ��NH3�����ʵ���Ũ�ȵı仯�������ͼ��ʾ��| c2(NH3) |
| c(N2)?c3(H2) |
| c2(NH3) |
| c(N2)?c3(H2) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| 5 |
| 7 |
| 5 |
| 7 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014ѧ�����ʡ�����и���12��ͳһ�������ۻ�ѧ�Ծ��������棩 ���ͣ������
��ҵ������ʱ�����ô�������Ӧ��SO2ת��ΪSO3��һ���ؼ����衣
��1��ij�¶��£�2SO2��g��+O2��g�� 2SO3��g�� ��H=-197 kj��mol����ʼʱ��10 L���ܱ������м���4��0 mol SO2��g����10��0 mol O2��g��������Ӧ�ﵽƽ��ʱ���ų�197kJ�����������¶��µ�ƽ�ⳣ��K= �������¶�K�� �������С�䡱����
2SO3��g�� ��H=-197 kj��mol����ʼʱ��10 L���ܱ������м���4��0 mol SO2��g����10��0 mol O2��g��������Ӧ�ﵽƽ��ʱ���ų�197kJ�����������¶��µ�ƽ�ⳣ��K= �������¶�K�� �������С�䡱����
��2��һ�������£���һ���������ܱ������г���2mol SO2��1mol O2���������з�Ӧ��
 2SO2��g��+O2��g��
2SO3��g�����ﵽƽ��ı�����������SO2��O2��SO3��ƽ��Ũ�ȶ���ԭ��������� ������ĸ����
2SO2��g��+O2��g��
2SO3��g�����ﵽƽ��ı�����������SO2��O2��SO3��ƽ��Ũ�ȶ���ԭ��������� ������ĸ����
A�����º��ݣ�����2mol SO3 B�����º��ݣ�����2mol N2
C�����º�ѹ������1 mol SO3 D�������¶�
��3����һ�ܱ������н������з�Ӧ��2SO2��g��+O2��g��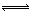 2SO3��g������ѧ��ȤС���ͬѧ̽����������������ʱ���ı�ijһ����ʱ��������Ӧ��Ӱ�죬������ʵ���������������й�ϵͼ�������ж�����ȷ���� ������ĸ����
2SO3��g������ѧ��ȤС���ͬѧ̽����������������ʱ���ı�ijһ����ʱ��������Ӧ��Ӱ�죬������ʵ���������������й�ϵͼ�������ж�����ȷ���� ������ĸ����
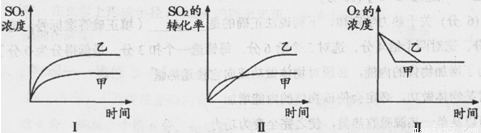
A��ͼ���о����Dz�ͬ�����Է�Ӧ��Ӱ�죬����ʹ�õĴ���Ч�ʽϸ�
B��ͼ���о�����ѹǿ�Է�Ӧ��Ӱ�죬�Ҽ�ѹǿ�ϸ�
C��ͼ���о������¶ȶԷ�Ӧ��Ӱ�죬���ҵ��¶Ƚϵ�
D��ͼ���о����Dz�ͬ�����Է�Ӧ��Ӱ�죬�Ҽ�ʹ�õĴ���Ч�ʽϸ�
��4��ijʵ��С����������ͼ��ʾװ���õ绯ѧԭ���������ᣬд��ͨ��SO2�ĵ缫�ĵ缫��Ӧʽ�� ��
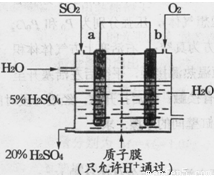
��5�����ղ�����SO2�����������ᡣ��֪25�桢101 kPaʱ��
SO2��g��+O2��g�� 2SO3��g�� ��H1=-197 kJ��mol��
2SO3��g�� ��H1=-197 kJ��mol��
H2O��g��=H2O��1�� ��H2=-44 kJ��mol��
2SO2��g��+O2��g��+2H2O��g��=2H2SO4��1�� H3=-545 kJ��mol��
д��SO3��g����H2O��1����Ӧ���Ȼ�ѧ����ʽ�� ��
��6����������Ƶ������Σ���һ���¶��£���K2SO4��Һ�еμ�Na2CO3��Һ��BaCl2��Һ�������ֳ�������ʱ��SO42-��CO32-��Ũ��֮�� ��[��֪���¶�ʱ��Ksp��BaSO4��=1��3x10-10��KsP��BaCO3��=5��2x10-9]��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com