


科目:高中化学 来源: 题型:阅读理解

| 序号 | 实验内容要点 | 实验现象, | 结论及解释 | ||||
| (1) | 加热后,缓慢通气体 | E中澄清石灰水不变浑浊,G中澄清石灰水变浑浊 | 猜想 ① ① 成立 | ||||
| (2) | 将D装置取走,连接好其余装置, 继续反应 |
观察到E中澄清石灰水始终不 变浑浊 |
猜想 ⑦ ⑦ 不成立 | ||||
| (3) | 用pH试纸测C中混和物pH | pH试纸变为 浅红或是红 浅红或是红 色,pH=3 |
猜想④成立. | ||||
| (4) | 取C中适量混和液,滴加稍过量 碳酸氢钠溶液蒸馏,取馏出物 碳酸氢钠溶液蒸馏,取馏出物 ,再与银氨溶液反应 |
出现银镜 | 猜想③成立,银镜反应离子方程式为 HCHO+2[Ag(NH3)2]++2OH-
HCHO+2[Ag(NH3)2]++2OH-
| ||||
| … | … | … |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
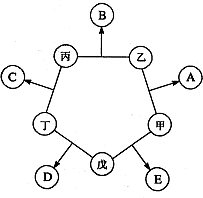 甲、乙、丙、丁、戊五种单质在一定条件下反应生成A、B、C、D、E五种化合物,其转化关系如图所示:又知:①甲、乙、丙、丁均为前三周期元素的单质,常温下均为气态,丙、丁是空气的主要成分,戊是日常生活中一种常见的金属.
甲、乙、丙、丁、戊五种单质在一定条件下反应生成A、B、C、D、E五种化合物,其转化关系如图所示:又知:①甲、乙、丙、丁均为前三周期元素的单质,常温下均为气态,丙、丁是空气的主要成分,戊是日常生活中一种常见的金属.查看答案和解析>>
科目:高中化学 来源: 题型:
| 甲 | 乙 | |
| 丙 | 丁 | 戊 |
| A、戊是两性元素 |
| B、五种元素中的金属元素中,丙的金属性最强 |
| C、简单离子半径:丙<丁 |
| D、甲的单质的熔点比丙单质的低 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com