

分析 (1)仪器X的名称是分液漏斗;
(2)用止水夹夹住C处橡皮管,向分液漏斗中加水,打开分液漏斗活塞,根据液体能否顺利流下判断气密性情况;
(3)二氧化锰和浓盐酸在加热条件下反应生成氯化锰、氯气和水,据此写出反应的离子方程式;
(4)氯气具有氧化性,能够将碘离子氧化成碘单质,据此判断装置Ⅳ中现象;
(5)干燥的氯气不具有漂白性,Ⅱ和Ⅲ之间可加干燥装置.
解答 解:(1)仪器X的名称是分液漏斗,故答案为:分液漏斗;
(2)加入药品前,检查I装置气密性的操作方法为:用止水夹夹住C处橡皮管,然后向分液漏斗中加水,打开分液漏斗活塞,液体不能顺利流下则气密性好,
故答案为:橡皮管,然后向分液漏斗中加水,打开分液漏斗活塞,液体不能顺利流下则气密性好;
(3)二氧化锰与浓盐酸反应制取氯气的离子方程式为:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O,
故答案为:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O;
(4)氯气具有氧化性,能够与碘化钾溶液反应生成碘单质,所以装置Ⅳ中通入氯气后,无色溶液变蓝色,反应的化学方程式为:Cl2+2KI=I2+2KCl,
故答案为:无色溶液变蓝色;
(5)干燥的氯气不具有漂白性,Ⅱ和Ⅲ之间可加干燥装置,除去氯气中的水蒸气,
故答案为:氯气中的水蒸气;在Ⅱ和Ⅲ之间可加浓硫酸干燥装置,来干燥Cl2.
点评 本题考查考查物质性质实验方案的设计,题目难度中等,涉及制取气体的装置及实验方案的设计、评价等知识点,综合性较强,明确氯气的制备原理及氯气的化学性质为解答关键,试题有利于培养学生的分析、理解能力及化学实验能力.


科目:高中化学 来源: 题型:推断题
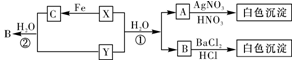
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硅 | B. | 硫 | C. | 铜 | D. | 铁 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
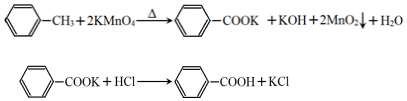
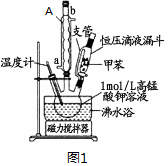
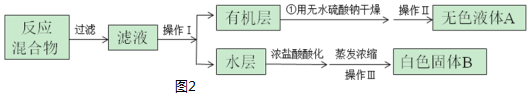
| 第一次 | 第二次 | 第三次 | 第四次 | |
| 体积(mL) | 24.00 | 24.10 | 22.40 | 23.90 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 质量为32g | B. | 含氧原子数为NA | ||
| C. | 含氧分子数为NA | D. | 在标准状况下,体积约为22.4L |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 标准状况下,22.4 L H2含有的原子数是2NA | |
| B. | 标准状况下,NA个水分子的体积是22.4 L | |
| C. | 任何情况下,1 mol CO中都含有NA个分子 | |
| D. | 通常状况下,NA个NH3分子的体积是22.4 L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙炔通入溴水中 | |
| B. | 乙烯通入酸性高锰酸钾溶液中 | |
| C. | 在镍作催化剂的条件下,苯与氢气反应 | |
| D. | 乙烷与氯气光照下发生反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com