
【题目】下列图示与对应的叙述相符的是

A.图1表示H2与O2发生反应过程中的能量变化,则H2的燃烧热为241.8 kJ·mol-1
B.图2表示压强对可逆反应2A(g)+2 B(g)![]() 3C(g)+D(s)的影响,乙的压强比甲的压强大
3C(g)+D(s)的影响,乙的压强比甲的压强大
C.图3表示等质量的钾、钠分别与足量水反应,则甲为钠
D.图4表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则相同条件下NaA溶液的pH大于同浓度的NaB溶液的pH
【答案】C
【解析】
试题分析:A、燃烧热是在一定条件下,1mol可燃物完全燃烧生成稳定的氧化物时所放出的热量,与图象不吻合,故A错误;B、该反应是一个反应前后气体体积减小的可逆反应,增大压强平衡向正反应方向移动,则反应物的含量减少,该图中改变条件后,反应物的含量不变,说明平衡不移动,加入的是催化剂,故B错误;C、钾比钠活泼,反应速率快。钠的摩尔质量小于钾的摩尔质量,在质量相等的条件下钠放出的氢气多,与图像吻合,故C正确;D、在稀释过程中HA的pH变化大,说明HA的酸性比HB强,越弱越水解,所以NaA的水解程度小于NaB,NaA与NaB水解显碱性,所以NaA溶液的pH小于同浓度的NaB溶液的pH,故D错误;故选C。


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:
【题目】填写下列空白:
(1)含有6.02×1023个H的H2O,其物质的量是________;1L1 mol /LNa2SO4溶液中含有______个Na+、______个SO![]() 。
。
(2)______mol H2O中含有的氧原子数与1.5 mol CO2中含有的氧原子数相等。
(3)将等物质的量的NH3和CH4混合,混合气体中NH3与CH4的质量比为________。
(4)要使NH3与CH4含相同数目的H原子,则NH3和CH4的物质的量之比为__________。
(5)标准状况下,密度为0.75 g·L-1的NH3与CH4组成的混合气体中,NH3的体积分数为__________,该混合气体对氢气的相对密度为________。
(6)已知a g A和b g B恰好完全反应生成0.2 mol C和d g D,则C的摩尔质量为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A. SiO2是一种空间立体网状结构的晶体,熔点高、硬度大
B. 石英坩埚不能用来熔融纯碱固体
C. 因SiO2不溶于水,故SiO2不是酸性氧化物
D. 氢氟酸能够刻蚀玻璃,故不能用玻璃瓶来盛装氢氟酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
①液溴易挥发,在存放液溴的试剂瓶中应加水封
②易燃试剂与强氧化性试剂分开放置并远离火源
③中和滴定实验时,用待测液润洗锥形瓶
④硅酸钠溶液应保存在带玻璃塞的试剂瓶中
A. ①② B. ①②③ C. ③④ D. ①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.PCl3分子是平面三角形,中心原子磷原子是sp2杂化
B.乙炔分子中的C原子是sp2杂化
C.凡中心原子采取sp3杂化的分子,其VSEPR模型都是四面体形
D.NH4Cl中有4种化学键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乌洛托品在合成、医药、染料等工业中有广泛用途,其结构简式如图所示。将甲醛水溶液与氨水混合蒸发可制得乌洛托品。若原料完全反应生成乌洛托品,则甲醛与氨的物质的量之比应为( )
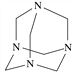
A. 1∶1 B. 2∶3
C. 3∶2 D. 2∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】偏二甲肼(C2H8N2)是一种高能燃料,燃烧产生的巨大能量可作为航天运载火箭的推动力.下列叙述正确的是()
A. 偏二甲肼(C2H8N2)的摩尔质量为60g
B. 6.02×1023个偏二甲肼(C2H8N2)分子的质量为60g
C. 1mol偏二甲肼(C2H8N2)的质量为60g/mol
D. 6g偏二甲肼(C2H8N2)含有NA个偏二甲肼(C2H8N2)分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,CO2与NH3反应可制得重要的化工产品三聚氰胺:3NH3 + 3CO2![]()
 +3H2O。
+3H2O。
(1)基态N原子的价层电子排布图为____________,三聚氰胺的几种组成元素中电负性由大到小的顺序为____________(用元素符号表示)。
(2)三聚氰胺中氮原子的杂化轨道类型为____________。
(3)上述合成三聚氰胺的反应过程中存在多种类型化学键的断裂与形成,但这些化学键中不包括____________(填选项字母)。
a.α键 b.π键 c.非极性共价键 d.极性共价键
(4)三聚氰胺的熔点为250 ℃,则其晶体类型是____________,又知硝基苯的熔点为5.7 ℃,异致这两种物质熔点差异的原因是____________。
(5)随者科学技术的发展,科学家们已合成了由碳、氧两种元素形成的原子晶体.其晶胞结构如图(a) 所示:若晶胞参数为a pm,设NA表示阿伏加德罗常数的值,则该晶胞的密度是____________ g cm-3。
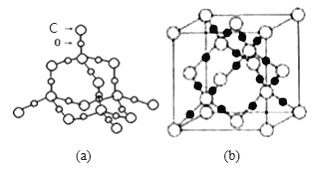
(6)SiO2晶体结构片断如图 (b)所示。通常人们把拆开1mol 某化学键所吸收的能量看成该化学键的键能。
化学键 | Si-O | Si-Si | O=O |
键能/ KJ·mol-1 | 460 | 176 | 498 |
Si(s)+O2(g)![]() SiO2(s),该反应的反应热△H = ___________
SiO2(s),该反应的反应热△H = ___________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com