
【题目】热激活电池可用作火箭、导弹的工作电源.一种热激活电池的基本结构如图所示,其中作为电解质的无水LiCl﹣KCl混合物受热熔融后,电池即可瞬间输出电能.该电池总反应为:PbSO4+2LiCl+Ca═CaCl2+Li2SO4+Pb.下列有关说法正确的是( ) 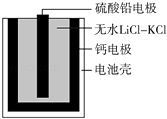
A.正极反应式:Ca+2Cl﹣﹣2e﹣═CaCl2
B.放电过程中,Li+向负极移动
C.每转移0.1 mol电子,理论上生成20.7 g Pb
D.常温时,在正负极间接上电流表或检流计,指针不偏转
【答案】D
【解析】解:A.正极发生还原反应,电极方程式为PbSO4+2e﹣+2Li+=Li2SO4+Pb,故A错误; B.放电过程中阳离子向正极移动,故B错误;
C.根据电极方程式PbSO4+2e﹣+2Li+=Li2SO4+Pb,可知每转移0.1 mol电子,理论上生成0.05molPb,质量为10.35g,故C错误;
D.常温下,电解质不是熔融态,离子不能移动,不能产生电流,因此连接电流表或检流计,指针不偏转,故D正确.
故选D.
由原电池总反应可知Ca为原电池的负极,被氧化生成反应H2(g)+Cl2(g)=2HCl(g),反应的电极方程式为Ca+2Cl﹣﹣2e﹣=CaCl2 , 为原电池的正极,发生还原反应,电极方程式为PbSO4+2e﹣+2Li+=Li2SO4+Pb,原电池工作时,阳离子向正极移动,阴离子向负极移动,结合电解方程式计算.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】图示中物质转化最终生成乙酸和高分子涂料胶黏剂Y的合成路线如下(部分反应条件已省略):
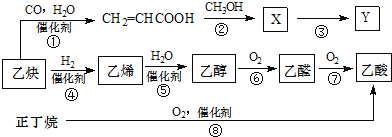
(1)化合物CH2═CHCOOH中所含官能团名称为_____________和____________;
(2)正丁烷的一种同分异构体的结构简式为_____________;Y的结构简式为_____________;
(3)图中8步反应中,原子利用率没有达到100%的为_____________(填序号)。
(4)写出下列反应的化学方程式(注明反应条件):反应⑥__________________________;反应⑧为(同时有水生成)_______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质的用途中,运用了物质的化学性质的是
A. 用胶状氢氧化铝凝聚水中的悬浮物进行净水
B. 用红棕色氧化铁制造红色油漆
C. 氢氧化铝作为医用的胃酸中和剂
D. 用氧化铝制造耐火坩埚和耐火管
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室有四个药品橱,已存放如下药品:
橱 | 甲橱 | 乙橱 | 丙橱 | 丁橱 |
药品 | 盐酸、硫酸 | CCl4、C2H5OH | 红磷、硫 | 铜、锌 |
实验室新购进一些活性炭,应将它存放在
A. 甲橱 B. 乙橱 C. 丙橱 D. 丁橱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下列反应的热化学方程式
6C(s)+5H2(g)+3N2(g)+9O2(g) 2C3H5(ONO2)3(l) ΔH1
2 H2(g)+ O2(g) 2H2O(g) ΔH2
C(s)+ O2(g) CO2(g) ΔH3
则反应4C3H5(ONO2)3(l) 12CO2(g)+10H2O(g)+O2(g)+6N2(g)的ΔH为
A. 12ΔH3+5ΔH2-2ΔH1 B. 2ΔH1-5ΔH2-12ΔH3
C. 12ΔH3-5ΔH2-2ΔH1 D. ΔH1-5ΔH2-12ΔH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各表述与示意图一致的是
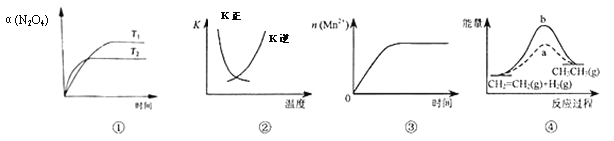
A. 图①表示N2O4(g)![]() 2NO2(g) ΔH>0,N2O4转化率随温度、时间的变化
2NO2(g) ΔH>0,N2O4转化率随温度、时间的变化
B. 图②中曲线表示反应2SO2(g)+O2(g)![]() 2SO3(g) ΔH<0,正、逆反应的平衡常数K随温度的变化
2SO3(g) ΔH<0,正、逆反应的平衡常数K随温度的变化
C. 图③表示10 mL0.01 mol/LKMnO4酸性溶液与过量0.1mol/LH2C2O4溶液混合时,n(Mn2+)随时间的变化
D. 图④中a、b曲线分别表示反应CH2=CH2(g)+H2(g)![]() CH3CH3(g) ΔH<0,使用和未使用催化剂时,反应过程中的能量变化
CH3CH3(g) ΔH<0,使用和未使用催化剂时,反应过程中的能量变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学反应2A(g)![]() B(g)+D(g)在四种不同条件下进行,B、D起始浓度为零,反应物A的浓度(mol/L)随反应时间(min)的变化情况,根据下述数据,完成下列填空:
B(g)+D(g)在四种不同条件下进行,B、D起始浓度为零,反应物A的浓度(mol/L)随反应时间(min)的变化情况,根据下述数据,完成下列填空:
实验 序号 | 温度/℃ | 时间/min | ||||||
0 | 10 | 20 | 30 | 40 | 50 | 60 | ||
1 | 800℃ | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
2 | 800℃ | c2 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
3 | 800℃ | c 3 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
4 | 820℃ | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
(1)在实验l过程中,10 min~20 min时间内用B表示该反应的平均化学反应速率为_________mol/(L·min)。
(2)在实验2过程中,A的初始浓度c2=______mol/L,反应经20min就达到平衡,可推测实验2中还隐含的条件是___________________________。
(3)设实验3的化学反应速率为v3,实验1的化学反应速率为v1,则v3_____v1,且c3________1.0 mol/L (填“<”、“>”或“=”)。
(4)比较实验4和实验l,可推测该反应是___________反应(填“吸热”或“放热”)。理由是______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列措施或事实不能用勒夏特列原理解释的是
A.新制的氯水在光照下颜色变浅
B.H2、I2、HI平衡混合气加压后颜色变深
C.往K2CrO4溶液中加酸,使溶液橙色加深
D.Fe(SCN)3溶液中加入几滴6mol/L NaOH溶液后溶液颜色变浅
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com