
【题目】某元素基态原子最外层的电子排布式如下,其中能表示该元素一定为主族元素的是( )
A.3s23p6B.ns2C.4s24p1D.4s1
科目:高中化学 来源: 题型:
【题目】根据下列实验现象,所得结论正确的是( )

实验 | 实验现象 | 结论 |
A | 左烧杯中铁表面有气泡,右边烧杯中铜表面有气泡 | 氧化性:Al3+>Fe2+>Cu2+ |
B | 左边棉花变为橙色,右边棉花变为蓝色 | 氧化性:Cl2>Br2>I2 |
C | 右烧杯中澄清石灰水变浑浊,左边烧杯中无明显变化 | 热稳定性:Na2CO3>NaHCO3 |
D | 锥形瓶中有气体产生,烧杯中液体变浑浊 | 非金属性:Cl>C>Si |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列过程中所发生的化学变化属于取代反应的是
A. 一定条件下乙醇和氧气反应生成乙醛 B. 乙烯通入溴水中
C. 乙烯合成聚乙烯 D. 光照射甲烷和氯气的混合气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一密闭容器中进行以下可逆反应:M(g)+N(g)![]() P(g)+2L在不同的条件下P的百分含量P %的变化情况如下图,则该反应( )
P(g)+2L在不同的条件下P的百分含量P %的变化情况如下图,则该反应( )

A. 正反应放热,L是固体
B. 正反应放热,L是气体
C. 正反应吸热,L是气体
D. 正反应放热,L是固体或气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】青蒿素,是烃的含氧衍生物,为无色针状晶体,易溶于丙酮、氯仿和苯中,在甲醇、乙醇、乙醚、石油醚中可溶解,在水中几乎不溶,熔点为156~157℃,热稳定性差,青蒿素是高效的抗疟药.已知:乙醚沸点为35℃.从青蒿中提取青蒿素的方法之一是以萃取原理为基础的,主要有乙醚浸取法和汽油浸取法.乙醚浸取法的主要工艺为:

请回答下列问题:
(1)对青蒿进行干燥破碎的目的是_____________________。
(2)操作I需要的玻璃仪器主要有:烧杯、_______________,操作Ⅱ的名称是___________________。
(3)操作Ⅲ的主要过程可能是___________________________(填字母)。
A.加水溶解,蒸发浓缩、冷却结晶
B.加95%的乙醇,浓缩、结晶、过滤
C.加入乙醚进行萃取分液
(4)用下列实验装置测定青蒿素分子式的方法如下:将28.2g青蒿素样品放在硬质玻璃管C中,缓缓通入空气数分钟后,再充分燃烧,精确测定装置E和F实验前后的质量,根据所测数据计算。
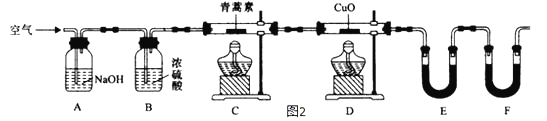
①装置E中盛放的物质是__________________,装置F中盛放的物质是____________________。
②该实验装置可能会产生误差,造成测定含氧量偏低,改进方法是______________________。
③用合理改进后的装置进行试验,称得:
装置 | 实验前/g | 实验后/g |
E | 22.6 | 42.4 |
F | 80.2 | 146.2 |
则测得青蒿素的最简式是_____________________________。
(5)某学生对青蒿素的性质进行探究。将青蒿素加入含有NaOH、酚酞的水溶液中,青蒿素的溶解量较小,加热并搅拌,青蒿素的溶解量增大,且溶液红色变浅,说明青蒿素与_________(填字母)具有相同的性质。
A.乙醇B.乙酸C.乙酸乙酯D.葡萄糖
(6)某科研小组经多次提取青蒿素实验认为用石油醚做溶剂较为适宜,实验中通过控制其他实验条件不变,来研究原料的粒度、提取时间和提取温度对青蒿素提取速率的影响,其结果如图所示:由下图可知控制其他实验条件不变,采用的最佳粒度、时间和温度为__________________。

A.80目、100分钟、50℃ B.60目、120分钟、50℃ C.60目、120分钟、55℃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是某兴趣小组通过实验获得的相同体积足量稀硫酸与铁反应的实验数据:
实验 序号 | 金属 质量/g | 金属 状态 | c(H2SO4) mol/L | 实验 温度/℃ | 金属消失 的时间/s |
1 | 0.10 | 丝 | 0.7 | 20 | 250 |
2 | 0.10 | 丝 | 1.0 | 20 | 200 |
3 | 0.10 | 粉末 | 1.0 | 20 | 125 |
4 | 0.10 | 粉末 | 1.0 | 30 | 50 |
分析上述数据,回答下列问题:
(1)①实验1、2可得出的结论是,硫酸浓度越_____,反应速率越慢;
②实验3、4可得出的结论是温度越_____,反应速率越快.
(2)①用铁粉和稀硫酸反应制取H2,实验过程中绘制出生成H2的体积(V)与时间(t)的关系如图所示. 试分析判断OE段、EF段、FG段、GH段反应速率(分别用v (OE)、v (EF)、v (FG)、v (GH)表示)最快时段是______.
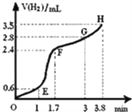
A.v (OE) B.v (EF)C.v (FG) D.v (GH)
②1min内反应较慢的原因是:_________;一段时间后反应明显加快的原因是_____.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】柠檬酸铁铵[(NH4)3Fe( C6 H5O7)2,摩尔质量488 g/mol] 是一种重要的食品添加剂。一种制备柠檬酸铁铵的实验步骤如下:

步骤1.在右图三颈烧瓶中加入16.7 g FeSO4·7H2O、40 ml.蒸馏水,3mL硫酸和1 g NaClO3,强力搅拌;
步骤2.升温至80℃,再补加l g NaClO3;
步骤3.向反应器中加入NaOH溶液,温度控制在80~90℃,剧烈搅拌;
步骤4.过滤,洗涤,沥干,得活性Fe(OH)3;
步骤5.将Fe(OH)3和一定量的水加入三颈烧瓶中,控制95℃以上,加入计算量的柠檬酸溶液,搅拌,并保温1h;
步骤6.冷却到50℃,搅拌下加入氨水40 mL,静置、浓缩至膏状,80℃干燥得柠檬酸铁铵24.9 g。
回答下列问题:
(1)步骤1发生反应的离子方程式为_____________________________。
(2)步骤2再补加NaClO3的目的是_____________________________。
(3)步骤3确定Fe3+已沉淀完全的方法是_____________________________。
(4)步骤4过滤时,所需硅酸盐质仪器除烧杯外,还需要_____________________________;证明Fe(OH)3已被洗涤干净的方法为__________________________。
(5)柠檬酸铁铵的产率为_________(结果保留三位有效数字)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com