
���̿����Ҫ�ɷ�ΪMnO2��������Al2O3��SiO2����п����Ҫ�ɷ�ΪZnS��������FeS��CuS��CdS���ʡ��������̿����п��Ϊԭ���Ʊ�MnO2��Zn������������£��м����Ĺ��岿���Ѿ���ȥ����
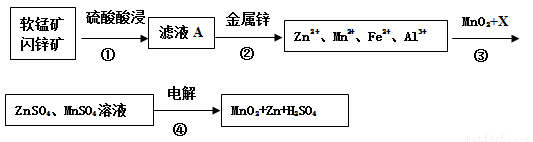
��֪�� ��ʯ�����н���Ԫ������ҺA�о���������ʽ���ڡ�
���ֽ���������ȫ������pH���±���
Zn2+ | Mn2+ | Fe2+ | Fe3+ | Al3+ | |
pH | 8.0 | 10.1 | 9.0 | 3.2 | 4.7 |
�ش��������⣺
��1���������Ϊ�˼ӿ�����Ľ�ȡ���ʣ��ɲ��õķ�����_________________����дһ�֣������з��������Ӧ������MnO2��FeS�����Ṳ��ʱ�е���ɫ������������Һ��Ϊ�ػ�ɫ��д��MnO2��FeS�����Ṳ�ȷ�����Ӧ�Ļ�ѧ����ʽ______________________��
��2������ڼ������п��Ϊ�˻��ս��������ս�������Ҫ�ɷ���_________��
��3���������MnO2����������__________________������һ������X������__________��
A��ZnO B��MgCO3 C��MnCO3 D��Cu(OH)2
��4��MnO2��Li����LiMnO2��������Ϊij����ӵ�ص��������ϣ���ط�Ӧ����ʽΪ�� Li1-xMnO2+LixC6=LiMnO2+6C��д��������ӵ�ص������缫��Ӧʽ__________��
��5����֪��HCN�ĵ��볣��K=4.9��10��10��H2S�ĵ��볣��K1=1.3��10�D7��K2=7.0��10�D15����NaCN��Һ��ͨ��������H2S���壬��Ӧ�����ӷ���ʽΪ__________________���ڷ�ˮ���������г���H2S��Mn2+ת��ΪMnS��ȥ������0.020 mol��L�D1Mn2+��ˮ��ͨ��һ������H2S���壬������Һ��pH=a����HS�DŨ��Ϊ1.0��10�D4 mol��L�D1ʱ��Mn2+��ʼ��������a=______��[��֪��Ksp(MnS)=1.4��10�D15]

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2017��ӱ�ʡ��������ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
ij�л�������Ľṹ��ʽ��ͼ��ʾ������˵����ȷ����( )

A�����ܷ���������Ӧ
B��1mol ������������2molBr2��Ӧ
C��1mol ������������4mol NaOH��Ӧ
D����NaHCO3��Na2CO3���ܷ�����Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ���½����ŵڶ�ʦ��ɽ��ѧ�߶���ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
ijͬѧ��ʵ�鱨���м�¼���������ݣ�������ȷ����( )
A. ��25 mL��Ͳ��ȡ12.36 mL����
B. ��pH��ֽ���ij��ҺpHΪ3.5
C. ��������ƽ��ȡ8.75 gʳ��
D. ����ʽ�ζ��ܲ��������������Ϊ15.60 mL
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�갲��ʡ�����и�һ��ѧ�ڵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
�������ӷ���ʽ��д��ȷ����( )
A. FeSO4��Һ��ϡ���ᷴӦ��3Fe2++NO3-+4H+=3Fe3++NO��+2H2O
B. ��������Һ�м���������ˮ��Al3++3OH-=Al(OH)3��
C. ��������ˮ��Cl2+H2O=2H++Cl-+ClO-
D. ̼����狀���������������Һ��Ӧ��NH4++OH-=NH3��H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�갲��ʡ�����и�һ��ѧ�ڵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
NA��ʾ�����ӵ�����������˵����ȷ����( )
A. 1mol��L-l Na2CO3��Һ�е�Na+��ĿΪ2NA
B. ��״���£�11.2 L CCl4����������Ϊ0.5NA
C. 5.6 g���ֱ������������ᡢ������Ӧ������ת��������Ϊ0.2NA
D. 1 mol Na������O2��Ӧ����Na2O��Na2O2��ʧȥNA����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ʡ�����С��˴���ѧ2017�������ѧ�ڿ�ѧ���������ۺ�-��ѧ�Ծ� ���ͣ�ѡ����
��NAΪ�����ӵ�������ֵ�������й�������ȷ���� ��������
A. �ڱ�״���£�22.4 L C2H6�к����ۼ�����ĿΪ6 NA
B. 5 g KHCO3��CaCO3��Ϲ�������������ĿΪ0.05 NA
C. �����£�1 L 0.1 mol��L�C1 CH3COONa��Һ��CH3COO��������ĿΪ0.1 NA
D. ��Na2O2��H2O�ķ�Ӧ�У���ת��0.2 NA������ʱ���ɵ�O2���Ϊ2.24 L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017���Ĵ�ʡ����12���¿���ѧ���������棩 ���ͣ������
�������������������������Ҫԭ��֮һ���������������ж��ַ�����
��1�������ü������ԭ���������֪��
CH4(g)��4NO2(g)��4NO(g)��CO2(g)��2H2O(g) ��H����574kJ/mol
CH4(g)��4NO(g)��2N2(g)��CO2(g)��2H2O(g) ��H����1160kJ/mol
��CH4(g)��NO2(g)��ԭΪN2(g)���Ȼ�ѧ����ʽ�� ��
��2��NH3����ԭ�������SCR)������ĿǰӦ����㷺���������������ѳ������������Ļ�ѧ��Ӧ�ǣ�2NH3(g)��NO(g)��NO2(g)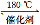 2N2(g)��3H2O(g)��H<0��Ϊ��ߵ��������ת���ʿɲ�ȡ�Ĵ�ʩ�ǣ�һ�����ɣ� ��
2N2(g)��3H2O(g)��H<0��Ϊ��ߵ��������ת���ʿɲ�ȡ�Ĵ�ʩ�ǣ�һ�����ɣ� ��
��3������β����������Ҫԭ��Ϊ��2NO(g)+2CO(g)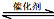 2CO2(g)+N2(g)����H��0
2CO2(g)+N2(g)����H��0
�ٸ÷�Ӧƽ�ⳣ������ʽ
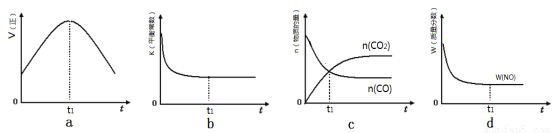
�����÷�Ӧ�ھ��ȡ����ݵ��ܱ���ϵ�н��У�����ʾ��ͼ��ȷ����˵����Ӧ�ڽ��е�t1ʱ�̴ﵽƽ��״̬���� ������ţ���
��4������ClO2�����������ﷴӦ�������£�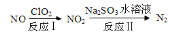
��Ӧ��Ļ�ѧ����ʽ��2NO+ClO2+H2O===NO2+HNO3+2HCl����Ӧ��Ļ�ѧ����ʽ�� ������11.2LN2���ɣ���״������������ClO2 g��
������11.2LN2���ɣ���״������������ClO2 g��
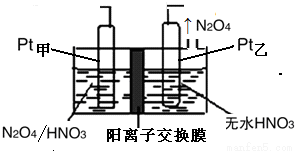
��5����ҵ�����к��е�NO2�����õ�ⷨ��������NO2Ϊԭ�Ͽ���������ɫ������N2O5���Ʊ�����֮һ���Ƚ�NO2ת��ΪN2O4Ȼ����õ�ⷨ�Ʊ�N2O5��װ������ͼ��ʾ��Pt��Ϊ�ĵ缫��Ӧʽ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�켪��ʡ���������ģ�⻯ѧ���������棩 ���ͣ�ѡ����
����ͼʾ���Ӧ��������ȷ����

A��ͼ��Ϊ��ˮ��Һ��H+��OH����Ũ�ȱ仯���ߣ�����ϡ�Ϳ�ʵ��a��b��ת��
B��ͼ��ΪH2O2���С������µķֽⷴӦ����b��ʾ�д���ʱ�ķ�Ӧ
C��ͼ���ɱ�ʾ��0.0110mol/L����ζ�0.0110mol/L��ˮʱ�ĵζ�����
D��ͼ��ΪNaCl�л�������KNO3����ȥKNO3���ڽϸ��¶����Ƶ�Ũ��Һ����ȴ�ᾧ�����ˡ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�������ʡĵ�����и���2�¿�ѧ������ۻ�ѧ�Ծ��������棩 ���ͣ������
��1����֪�ڳ��³�ѹ�£�
��CH3CH2OH(l)+3O2(g) 2CO2(g)+3H2O(g) ��H1=-1366kJ��mol��1
2CO2(g)+3H2O(g) ��H1=-1366kJ��mol��1
��2CO(g)+O2(g)=2CO2(g) ��H2
��H2O(g)=H2O(l) ��H3=-44kJ��mol��1
��CH3CH2OH(l)+2O2(g) 2CO(g)+3H2O(l) ��H4=-932kJ��mol��1
2CO(g)+3H2O(l) ��H4=-932kJ��mol��1
�� CO��ȼ���� ��H =_________��
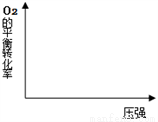
��ͼ�л�������ͬ�¶��£�T1>T2����������Ӧ����O2��ƽ��ת������ѹǿ�仯�Ĺ�ϵͼ������ͼ�ϱ�ע�¶�T1��T2����_________
��3��һ�������£������Ϊ3 L���ܱ������з�ӦCO(g) + 2H2(g)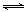 CH3OH(g)�ﵽ��ѧƽ��״̬��
CH3OH(g)�ﵽ��ѧƽ��״̬��
�ٷ�Ӧ��ƽ�ⳣ������ʽK=__________��������ͼ�������¶ȣ�Kֵ��___________�����������С�����䡱����
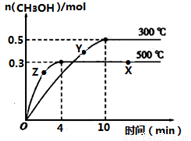
��500��ʱ���ӷ�Ӧ��ʼ���ﵽ��ѧƽ�⣬��H2��Ũ�ȱ仯��ʾ�Ļ�ѧ��Ӧ������________��
��X����Y���ƽ�����ʣ�v(X)_________v(Y)������X�������Ӧ����v��(X)��Z����淴Ӧ����v��(Z)�Ĵ�С��ϵΪv��(X)________v��(Z)�������������������=������
��300��ʱ�ܹ�˵���ÿ��淴Ӧ�ﵽ��ѧƽ��״̬�ı�־��____________ ������ĸ����
a��v����(CH3OH) = v����(H2) b�����������ܶȲ��ٸı�
c����������ƽ����Է����������ٸı� d��CO��H2��CH3OH��Ũ�����
��500��ʱ�����������ݻ�ѹ����ԭ����1/2���������������������£���ƽ����ϵ������Ӱ����___________��������ĸ��
a��c��H2������ b������Ӧ���ʼӿ죬�淴Ӧ���ʼ���
c��CH3OH �İٷֺ������� d������ƽ��ʱc(H2)/ c(CH3OH)��С
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com