
在下列给定条件的溶液中,一定能大量共存的离子组是 ( )。
A.无色溶液:Ca2+、H+、Cl-、HSO3-
B.能使pH试纸呈红色的溶液:Na+、NH4+、I-、NO3-
C.FeCl2溶液:K +、Na+、SO42-、AlO2-
+、Na+、SO42-、AlO2-
D.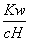 =0.1 mol·L-1的溶液:Na+、K+、SiO32-、NO3-
=0.1 mol·L-1的溶液:Na+、K+、SiO32-、NO3-
科目:高中化学 来源: 题型:
用惰性电极电解下列溶液一小段时间后,加入一定量的另一种物质(括号内),溶液能与原来溶液完全一样的是 ( )
A.CuSO4[Cu(OH)2] B.NaOH(NaOH)
C.NaCl(NaCl) D.CuCl2(CuCl2)
查看答案和解析>>
科目:高中化学 来源: 题型:
可用来鉴别己烯、甲苯、乙酸乙酯和苯酚溶液的一组试剂是
A. 溴水、氯化铁溶液 B. 溴水、酸性高锰酸钾溶液
C. 溴水、碳酸钠溶液 D. 氯化铁溶液、酸性高锰酸钾溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
将AgCl分别加入盛有:①5 mL水;②6 mL 0.5 mol·L-1 NaCl溶液;③10 mL 0.2 mol·L-1 CaCl2溶液;④50 mL 0.1 mol·L-1盐酸的烧杯中,均有固体剩余,各溶液中c(Ag+)从大到小的顺序排列正确的是 ( )。
A.④③②① B.②③④① C.①④③② D .①③②④
.①③②④
查看答案和解析>>
科目:高中化学 来源: 题型:
难溶性杂卤石(K2SO4·MgSO4·2CaSO4·2H2O)属于“呆矿”,在水中存在如下平衡:
K2SO4·MgSO4·2CaSO4·2H2O(s)2Ca2+(aq)+2K+(aq)+Mg2+(aq)+4SO42-(aq)+2H2O
为 能充分利用钾资源,用饱和Ca(OH)2溶液溶浸杂卤石制备硫酸钾,工艺流程
能充分利用钾资源,用饱和Ca(OH)2溶液溶浸杂卤石制备硫酸钾,工艺流程 如下:
如下:

(1)滤渣主要成分有________和________以及未溶杂卤石。
(2)用化学平衡移动原理解释Ca(OH)2溶液能溶解杂卤石浸出K+的原因:________________________________________________________________________。
(3)“除杂”环节中,先加入________溶液,经搅拌等操作后,过滤,再加入________溶液调滤液pH至中性。
 (4)不同温度下,K+的浸出浓度与溶浸时间的关系如图。由图可得,随着温度升高,①_________,
(4)不同温度下,K+的浸出浓度与溶浸时间的关系如图。由图可得,随着温度升高,①_________,
②________________________________________
________________________________________。
(5)有人以可溶性碳酸盐为溶浸剂,则溶浸过程中会发生:CaSO4(s)+CO32-CaCO3(s)+SO42-
已知298 K时,Ksp(CaCO3)=2.80×10-9,
Ksp(CaSO4 )=4.90×10-5,求此温度下该反应的平衡常数K
)=4.90×10-5,求此温度下该反应的平衡常数K (计算结果保留三位有效数字)。
(计算结果保留三位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
常见的五种盐A、B、C、D、E,它们的阳离子可能是Na+、NH4+、Cu2+、Ba2+、Al3+、 Ag+、Fe3+,阴离子可能是Cl-、NO3-、SO42-、CO32-,已知:
Ag+、Fe3+,阴离子可能是Cl-、NO3-、SO42-、CO32-,已知:
①五种盐均溶于水,水溶液均为无色。
②D的焰色反应呈黄色。
③A的溶液呈中性,B、C、E的溶液呈酸性,D的溶液呈碱性。
④若在这五种盐的溶液中分别加入Ba(NO3)2溶液,只有A、C的溶液不产生沉淀。
⑤若在这五种盐的溶液中,分别加入氨水,E和C的溶液中生成沉淀,继续加氨水,C中沉淀消失。
⑥把A的溶液分别加入到B、C、E的溶液中,均能生成不溶于稀硝酸的沉淀。
请回答下列问题。
(1)五种盐中,一定没有的阳离子是________;所含阴离子相同的两种盐的化学式是________。
(2)D的化学式为________,D溶液显碱性的原因是(用离子方程式表示)_______________________________________________________________
________________________________________________________________。
(3)A和C的溶液反应的离子方程式是________;E和氨水反应的离子方程式是________________________________________________________ _____。
_____。
(4)若要检验B中所含的阳离子,正确的实验方法是______________________
_________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
由C、H、O三种元素组成的化合物8.8 g,完全燃烧后得到CO2 22.0 g,H2O 10.8 g,该化合物的实验式是( )
A.C5H6O B.C5H12O C.C5H12O2 D.C5H10O
查看答案和解析>>
科目:高中化学 来源: 题型:
下列变化过程中表示的能量转化关系错误的是( )
A.植物光合作用:光能→生物质能 B.木柴烧饭:生物质能→热能
C.电灯发光:电能→化学能 D.太阳能热水器:光能→热能
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D四种短周期元素。原子序数依次增大,A原子的最外层上有4个电子;B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体甲;D的L层电子数等于K、M两个电子层上的电子数之和。
(1)写出下列元素的名称:A_______,B ,C_______,D 。
(2)D的质子数和中子数相等,D的原子组成符号为 ,它的最高价为___________价。
(3)用电子式表示A、D两元素形成AD2的过程: ;
写出C2B2的电子式 。
(4)氢元素与B、D 均可以形成原子个数比为2:1的化合物,H2B的熔沸点高于H2D的原因是
。
(5)写出甲和A的最高价氧化物反应的化学方式: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com